
分析 (1)驗證碳酸、醋酸、硅酸的酸性強弱,將CH3COOH與Na2CO3發生反應:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,說明酸性CH3COOH>H2CO3;產生的CO2氣體先通過飽和的碳酸氫鈉溶液除去混有的醋酸蒸汽,然后再通入硅酸鈉溶液發生反應CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓,說明酸性H2CO3>H2SiO3,再結合儀器的作用畫圖;
(2)根據操作步驟排序,再根據物質間的反應及物質的性質確定實驗現象及結論.
解答 解:(1)驗證碳酸、醋酸、硅酸的酸性強弱,將CH3COOH與Na2CO3發生反應:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,說明酸性CH3COOH>H2CO3;產生的CO2氣體先通過飽和的碳酸氫鈉溶液除去混有的醋酸蒸汽,然后再通入硅酸鈉溶液發生反應CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓,說明酸性H2CO3>H2SiO3;D中為醋酸,A為碳酸鈉,醋酸滴加到A中與Na2CO3反應生成二氧化碳,B中為飽和碳酸氫鈉溶液,除去二氧化碳中混有的醋酸蒸汽,二氧化碳與通入C中與硅酸鈉反應生成硅酸,所以簡易的裝置圖見答案,
答:簡易的裝置圖為 ;
;
(2)實驗時,實驗操作步驟為:連接裝置、檢查氣密性、加入藥品和試劑、打開分液漏斗的蓋子并打開活塞,醋酸和碳酸鈉反應Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑,A中固體表面有氣泡產生,說明酸性CH3COOH>H2CO3;乙酸易揮發,產生的CO2氣體先通過飽和的碳酸氫鈉溶液除去混有的醋酸蒸汽,然后再通入試管C硅酸鈉溶液發生反應CO2+H2O+Na2SiO3=Na2CO3+H2SiO3↓,反應生成碳酸鈉和硅酸沉淀,所以看到有沉淀生成,說明酸性H2CO3>H2SiO3,酸性CH3COOH>H2CO3>H2SiO3,
答:A中固體表面有氣泡產生;說明酸性CH3COOH>H2CO3;試管C中有白色沉淀生成;說明酸性H2CO3>H2SiO3;酸性CH3COOH>H2CO3>H2SiO3.
點評 本題考查了探究順序強弱實驗方案的設計,明確物質的性質是解本題關鍵,結合強酸制取弱酸實驗原理來分析解答,注意:醋酸有揮發性,導致制取的二氧化碳中含有醋酸,干擾實驗,為易錯點,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 在蔗糖中加入濃硫酸后出現發黑現象,說明濃硫酸具有脫水性 | |
| B. | 濃硝酸在光照條件下顏色變黃,說明濃硝酸不穩定 | |
| C. | 常溫下濃硫酸、濃硝酸可以用鋁罐儲存,說明濃硫酸、濃硝酸與鋁不反應 | |
| D. | 反應CuSO4+H2S═CuS↓+H2SO4說明硫化銅既不溶于水,也不溶于稀硫酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 甲烷分子中的4個氫原子都可以被取代,若甲烷分子中的4個氫原子都被苯基取代,可以得到的分子如圖,對該分子的描述,不正確的是( )
甲烷分子中的4個氫原子都可以被取代,若甲烷分子中的4個氫原子都被苯基取代,可以得到的分子如圖,對該分子的描述,不正確的是( )| A. | 分子式為C25H20 | |
| B. | 所有的碳原子不可能都在同一平面上 | |
| C. | 所有原子一定在同一平面上 | |
| D. | 此物質屬于芳香烴類物質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L Cl2溶于水,轉移的電子數目小于 NA | |
| B. | 常溫常壓下,18 g H2O中含有的原子總數為3 NA | |
| C. | 0.1 moI•L-1的CH3COOH溶液中所含的離子和分子總數為0.1NA | |
| D. | 乙烯和聚乙烯組成的14 g混合物中原子總數為3 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
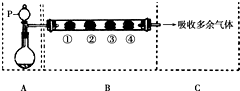 用如圖裝置可以完成一系列實驗(圖中夾持裝置已略去).請回答下列問題:
用如圖裝置可以完成一系列實驗(圖中夾持裝置已略去).請回答下列問題:| B中棉花的位置 | ① | ② | ③ | ④ |
| 所蘸試劑 | 石蕊試液 | 品紅溶液 | 淀粉和碘 水混合液 | 氫硫酸 |
| 現象 | a | b | 褪色 | 淺黃色 |
| 體現SO2的性質 | c | d | e | f |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com