
【題目】根據反應KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)設計如下原電池,其中甲、乙兩燒杯中各物質的物質的量濃度均為1 mol·L-1,溶液的體積均為200 mL,鹽橋中裝有飽和K2SO4溶液。下列說法不正確的是( )

A.石墨b是原電池的負極,發生氧化反應
B.忽略溶液體積變化,Fe2(SO4)3濃度變為1.5 mol/L,則反應中轉移的電子為0.1 mol
C.甲燒杯中的電極反應式:MnO4-+5e-+8H+=Mn2++4H2O
D.電池工作時,鹽橋中的K+向甲燒杯中移動
 各地期末復習特訓卷系列答案
各地期末復習特訓卷系列答案 小博士期末闖關100分系列答案
小博士期末闖關100分系列答案科目:高中化學 來源: 題型:
【題目】下列有關溶液中粒子濃度的關系式中,正確的是( )

A.pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸強堿鹽NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.圖中a點溶液中各離子濃度的關系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
D.圖中pH=7時:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】苯乙烯是一種重要的化工原料,可采用乙苯催化脫氫法制備,反應如下: ![]() (g)
(g)![]()
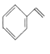 (g)+H2(g) △H=+17.6kJ/mol。
(g)+H2(g) △H=+17.6kJ/mol。
(1)從溫度和壓強角度分析提高乙苯平衡轉化率可采取的措施有___________。
(2)工業上,通常在乙苯蒸氣中摻混水蒸氣(原料氣中乙苯和水蒸氣的物質的量之比為1:4),測得容器總壓和乙苯轉化率隨時間變化結果如圖所示。
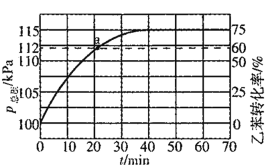
①摻入水蒸氣能提高乙苯的平衡轉化率,解釋說明該事實__________。
平衡常數Kp=_______kPa(Kp為以分壓表示的平衡常數)
②反應速率V=V正-V逆=k正P乙苯-k逆p苯乙烯p氫氣,k正、k逆分別為正逆反應速率常數。計算a處的![]() ______。
______。
(3)CO2氣氛下乙苯催化脫氫可同時存在圖1兩種途徑:
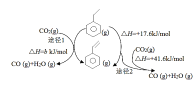
①b=_______kJ/mol。
②途徑I的反應歷程圖所示,下列說法正確的是______________。
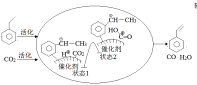
a.CO2為氧化劑
b.狀態1到狀態2形成了O-H鍵
c.中間產物只有(![]() )
)
d.該催化劑可提高乙苯的平衡轉化率
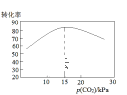
③在相同的容器中,不同p(CO2)的條件下,進行相同的反應時間,p(CO2)與乙苯轉化率關系如圖,分析,p(CO2)為15kPa時乙苯轉化率最高的因____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Na2S可用于制造硫化染料、沉淀水體中的重金屬等。
(1)Na2S溶液中S2-水解的離子方程式為_________。
(2)室溫時,幾種重金屬離子的硫化物的溶度積常數如下表:
金屬硫化物 | FeS | PbS | CuS | HgS |
Ksp | 6.3×10-18 | 1.0×10-28 | 6.3×10-36 | 1.6×10-52 |
①向物質的量濃度相同的Fe2+、Pb2+、Cu2+、Hg2+的混合稀溶液中,逐滴加入Na2S稀溶液,首先沉淀的離子是____。
②用Na2S溶液沉淀廢水中Pb2+,為使Pb2+沉淀完全[c(Pb2+)≤1×10-6mol/L],則應滿足溶液中c(S2-)≥_____mol/L。
③反應Cu2+(aq)+FeS(s)![]() Fe2+(aq)+CuS(s)的平衡常數K=_______。
Fe2+(aq)+CuS(s)的平衡常數K=_______。
(3)測定某Na2S和NaHS混合樣品中兩者含量的實驗步驟如下:
步驟1.準確稱取一定量樣品于燒杯中,加入少量蒸餾水溶解,轉移至500mL容量瓶中定容。
步驟2.準確移取25.00mL上述溶液于錐形瓶中,加入茜素黃GG-百時香酚藍混合指示劑,用0.2500mol/L鹽酸標準溶液滴定(Na2S+HCl=NaHS+NaCl)至終點,消耗鹽酸24.00mL;向其中再加入5mL中性甲醛(NaHS+HCHO+H2O→NaOH+HSCH2OH)和3滴酚酞指示劑,繼續用0.2500mol/L鹽酸標準溶液滴定(NaOH+HCl=NaCl+H2O)至終點,又消耗鹽酸34.00mL。
計算原混合物中Na2S與NaHS的物質的量之比(寫出計算過程)___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某紅色固體粉末樣品可能含有Fe2O3和Cu2O中的一種或兩種,某校化學自主探究實驗小組擬對其組成進行探究。
查閱資料:Cu2O在酸性溶液中會發生反應:Cu2O+2H+=Cu+Cu2++H2O
探究一:用如圖所示裝置進行實驗,回答下列問題:

(1)儀器組裝完成后,夾好止水夾,_____,則說明裝置A的氣密性良好.
(2)裝置A是氫氣的發生裝置,可以選用的藥品是________(填選項)
A.稀硫酸和鋅片B.稀硝酸和鐵片 C.氫氧化鈉溶液和鋁片D.濃硫酸和鎂片
(3)從下列實驗步驟中,選擇正確的操作順序:①________③(填序號).
①打開止水夾②熄滅C處的酒精噴燈 ③C處冷卻至室溫后,關閉止水夾
④點燃C處的酒精噴燈 ⑤收集氫氣并驗純⑥通入氣體一段時間,排盡裝置內的空氣
探究二:
(4)甲同學取少量樣品于試管中,加入適量的稀硫酸,若無紅色物質生成,則說明樣品中不含Cu2O;乙同學認為觀點不正確,其原因是_____________;丙同學另取少量樣品于試管中,加入適量的濃硝酸,產生紅棕色的氣體.證明樣品中一定含有________,其反應的離子方程式為_____;丁同學預設計實驗證明另一種物質是否存在,其方案為__________。
(5)取一定量樣品于燒杯中,加入足量的稀硫酸,若反應后經過濾得到固體3.2g,濾液中Fe2+有1.0mol,則樣品中n(Cu2O)=_________mol.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵及其化合物在生活、生產中有廣泛應用。請回答下列問題:
(1)在實驗室中,![]() 可用鐵粉和______反應制備,
可用鐵粉和______反應制備,![]() 可用鐵粉和______反應制備。
可用鐵粉和______反應制備。
(2)黃鐵礦![]() 主要成分為
主要成分為![]() 是生產硫酸和冶煉鋼鐵的重要原料。高溫下可發生反應:
是生產硫酸和冶煉鋼鐵的重要原料。高溫下可發生反應:
![]() ,該過程中若有
,該過程中若有![]()
![]() 參加反應,則反應過程中轉移______mol電子。
參加反應,則反應過程中轉移______mol電子。
(3)![]() 與Zn組成新型二次電池高鐵電池,電解液為堿溶液,其反應式為:
與Zn組成新型二次電池高鐵電池,電解液為堿溶液,其反應式為:![]() ,放電時電池的負極反應式為______;充電時電解液的pH______
,放電時電池的負極反應式為______;充電時電解液的pH______![]() 填“增大”“減小”或“不變”之一
填“增大”“減小”或“不變”之一![]() 。
。
(4)某同學向盛有![]() 溶液的試管中加入幾滴酸化的
溶液的試管中加入幾滴酸化的![]() 溶液,溶液變成棕黃色,發生反應的離子方程式為______;一段時間后,溶液中有氣泡出現,并放熱,隨后有紅褐色沉淀生成。產生氣泡的原因是______;生成沉淀的原因是______
溶液,溶液變成棕黃色,發生反應的離子方程式為______;一段時間后,溶液中有氣泡出現,并放熱,隨后有紅褐色沉淀生成。產生氣泡的原因是______;生成沉淀的原因是______![]() 用平衡移動原理解釋
用平衡移動原理解釋![]() 。
。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗不能達到預期目的是

A.實驗①:擠出膠頭滴管中的NaOH溶液,觀察Fe(OH)2沉淀的顏色
B.實驗②:繼續煮沸溶液至紅褐色,停止加熱,當光束通過體系時產生丁達爾效應
C.實驗③:通過觀察酸性KMnO4溶液紫色褪去,確認有乙烯生成
D.實驗④:控制一定溫度,將石油分離為汽油、柴油等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從工業廢釩中回收金屬釩既避免污染環境又有利于資源綜合利用。某工業廢釩的主要成分為V2O5、VOSO4和SiO2等,下圖是從廢釩中回收釩的一種工藝流程:

(1)為了提高“酸浸”效率,可以采取的措施有________(填兩種).
(2)“還原”工序中反應的離子方程式為________.
(3)“沉釩”得到NH4VO3沉淀,需對沉淀進行洗滌,檢驗沉淀完全洗凈的方法是________.
(4)寫出流程中鋁熱反應的化學方程式________.
(5)電解精煉時,以熔融NaCl、CaCl2和VCl2為電解液(其中VCl2以分子形式存在).粗釩應與電源的________極(填“正”或“負”)相連,陰極的電極反應式為________.
(6)為預估“還原”工序加入H2C2O4的量,需測定“酸浸”液中VO2+的濃度.每次取25.00mL“酸浸”液于錐形瓶用a mol/L(NH4)2Fe(SO4)2標準溶液和苯代鄰氨基苯甲酸為指示劑進行滴定(其中VO2+ VO2+),若三次滴定消耗標準液的體積平均為bmL,則VO2+的濃度為________g/L(用含a、b的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
銅礦( CuFeS2)是煉銅的最主要礦物。火法冶煉黃鋼礦的過程中,其中一步反應是:2Cu2O+Cu2S![]() 6Cu+SO2。回答下列問題。
6Cu+SO2。回答下列問題。
(1)Cu+價電子的電子排布圖為___________,Cu2O與Cu2S比較,熔點較高的是___________,原因為______________________。
(2)SO2與SO3的鍵角相比,鍵角更小的是___________。某種硫的氧化物冷卻到289.8K時凝固得到一種螺旋狀單鏈結構的固體,其結構片段如圖1所示。此固態物質中S原子的雜化軌道類型是___________;該物質的化學式為___________。

(3)離子化合物CaC2的晶體結構如圖2所示。寫出該物質的電子式___________。從鈣離子看該晶體屬于___________堆積,一個晶胞含有的π鍵平均有___________個。

(4)根據圖3可知,與每個C60分子距離最近且相等的C60分子有___________個,其距離為___________cm(列出計算式即可)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com