
分析 ①根據影響化學平衡因素結合速率大小分析判斷反應前后的體積變化;
②反應前后系數相同,改變壓強平衡移動說明反應物中含有固體或純液體;
③固體和純液體對平衡無影響;
④縮小容器體積,C的濃度首先變大,顏色變深,平衡向氣體體積縮小的方向移動,顏色變淺,但溫度不變,平衡常數不變.
解答 解:①反應mA+nB?pC,若A、B、C都是氣體,減壓后正反應速率小于逆反應速率,證明逆向反應是氣體體積增大的反應,得到m+n>p,
故答案為:m+n>p;
②若反應mA+nB?pC;C為氣體,且m+n=p,在加壓時化學平衡發生移動,說明AB中至少有一種是固體或純液體,加壓平衡逆向進行,
故答案為:逆;
③若反應mA+nB?pC;如果在體系中增加或減少B的量,平衡均不發生移動,證明B一定是固體或純液體,不是氣體,
故答案為:氣;
④縮小容器體積,C的濃度首先變大,顏色變深,平衡向氣體體積縮小的方向移動,顏色變淺,但溫度不變,平衡常數不變,故答案為:先變深,后逐漸變淺;不變.
點評 本題考查了化學平衡的影響因素判斷,主要考查壓強對平衡的影響和物質性質的判斷,化學平衡的移動規律是解題的關鍵.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
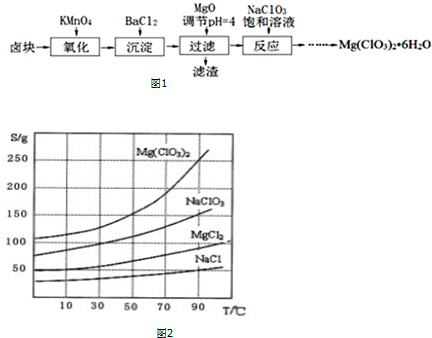
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
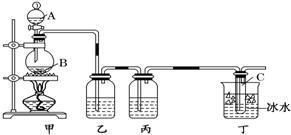
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
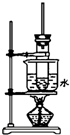 如圖是實驗室制取酚醛樹脂的裝置圖(燒杯底部墊有石棉網).
如圖是實驗室制取酚醛樹脂的裝置圖(燒杯底部墊有石棉網).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在常溫常壓下11.2 L氫氣所含的原子數目為NA | |
| B. | 18 g水所含的氫原子數目為NA | |
| C. | 2.3 g金屬鈉轉化為Na2O和Na2O2的混合物時失去的電子數為0.1NA | |
| D. | 物質的量濃度為0.5 mol•L-1 的MgCl2溶液,含有的Cl- 數為1 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑥⑦ | B. | ②⑤⑥⑦ | C. | ①③④⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com