
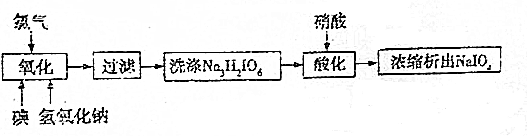
分析 ①單質碘與氯氣、氫氧化鈉反應:I2+2NaOH+7Cl2═2Na3H2IO6+14NaCl+8H2O,洗滌是除去沉淀上附著的雜質;
②硝酸酸化時生成硝酸鈉和高碘酸鈉;
③根據化學方程式書寫.
解答 解:①單質碘與氯氣、氫氧化鈉反應:I2+2NaOH+7Cl2═2Na3H2IO6+14NaCl+8H2O,洗滌是除去沉淀上附著的雜質,由方程式可知,雜質為NaCl,所以洗滌Na3H2IO6沉淀時,主要是除去氯化鈉;
故答案為:氯化鈉;
②硝酸酸化時生成硝酸鈉和高碘酸鈉,所以硝酸酸化得到的另一鹽類副產物為硝酸鈉;
故答案為:NaNO3;
③單質碘與氯氣、氫氧化鈉反應:I2+2NaOH+7Cl2═2Na3H2IO6+14NaCl+8H2O,則其離子方程式為:I2+2NaOH+7Cl2═2Na3H2IO6+14NaCl+8H2O;
故答案為:I2+2NaOH+7Cl2═2Na3H2IO6+14NaCl+8H2O.
點評 本題考查了物質的制備流程,題目難度不大,注意分析物質的制備流程是解題的關鍵,側重于考查學生的分析能力.


科目:高中化學 來源: 題型:選擇題
| A. | 1mol任何氣體的體積都約為22.4L | |
| B. | 22.4L水在標況下的質量為18g | |
| C. | 2L 1mol/L Na2CO3溶液中Na+濃度為4mol/L | |
| D. | 從1L NaCl溶液中取出100mL,其濃度與原1L溶液相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電解質溶液的濃度增大,pH減小 | B. | 電解質溶液的濃度增大,pH增大 | ||
| C. | 電解質溶液的濃度減小,pH減小 | D. | 電解質溶液的濃度不變,pH不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單位時間內生成nmolA2,同時消耗2n molAB | |
| B. | 容器內3種氣體共存 | |
| C. | AB的消耗速率等于A2的消耗速率 | |
| D. | 容器中各組分的體積分數不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子序數越大,原子半徑一定越大 | |
| B. | 電子層數多的原子半徑一定比電子層數少的原子半徑大 | |
| C. | 元素性質的周期性變化不是元素性質的簡單重復 | |
| D. | 按C、N、O、F的順序,元素的最高正價依次升高 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 分解高錳酸鉀制取氧氣后,殘留在試管內壁上的黑色物質可用濃鹽酸洗滌 | |
| B. | 失去標簽的AgNO3溶液、稀鹽酸、NaOH溶液、AlCl3溶液可選用(NH4)2CO3 溶液作鑒別試劑 | |
| C. | 用銅絲代替鉑絲做焰色反應 | |
| D. | 把SO2氣體通入酸性KMnO4溶液中,KMnO4溶液的顏色褪去,即可證明SO2具有漂白性 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學卷(解析版) 題型:選擇題
能降低反應所需的活化能的是( )
A.降低溫度 B.使用催化劑 C.增大壓強 D.增加濃度
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省高二上10月階段測化學卷(解析版) 題型:選擇題
下列變化過程不能直接實現的是
①HCl ②Cl2 ③Ca(ClO)2 ④HClO ⑤CO2
A.①→② B.②→③ C.③→④ D.④→⑤
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com