
| 1.5mol |
| 4mol |
| C(C) 3 |
| C(A)C(B) 2 |
| C(C) 3 |
| C(A)C(B) 2 |


科目:高中化學 來源: 題型:
| O2 |
| 催化劑/△ |
| H2O |
| NaOH |
| 鹽酸 |
| 鹽酸 |
| 電解 |
| O2 |
| △ |
| CO2 |
| A、②④ | B、③④ | C、①④ | D、①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
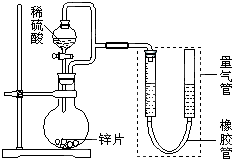 某同學設計了如圖所示裝置(部分夾持裝置已略去)進行實驗研究.據此回答下列問題:
某同學設計了如圖所示裝置(部分夾持裝置已略去)進行實驗研究.據此回答下列問題:| 序號 | V(H2SO4)/mL | c(H2SO4)/mol?L-1 | t/s |
| Ⅰ | 40 | 1 | t1 |
| Ⅱ | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、糖類、油脂和蛋白質是基本營養物質 |
| B、蛋白質水解的最終產物是多肽 |
| C、糖尿病人不能食用含糖和淀粉的食品 |
| D、向蛋白質溶液中加入濃的Na2SO4或CuSO4溶液均可使蛋白質鹽析而分離提純 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| A、容器I、Ⅲ中平衡常數相同 |
| B、容器II、Ⅲ中正反應速率始終相同 |
| C、容器Ⅱ、Ⅲ中的反應達平衡時,SO3的體積分數:II>III |
| D、容器I中SO2的轉化率與容器Ⅱ中SO3的轉化率之和等于1 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、丙烷完全燃燒的熱化學方程式為C3H8+5O2═3CO2+4H2O△H=-2 036 kJ/mol |
| B、C3H8(g)+5O2(g)═3CO2(g)+4H2O(g);△H<-2 036 kJ/mol |
| C、丙烷完全燃燒的熱化學方程式為:C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=2 036 kJ/mol |
D、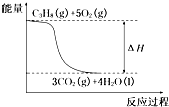 丙烷燃燒的能量變化可用如圖所示表示 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com