
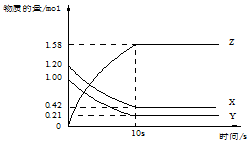
 一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:下列描述正確的是( )
一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:下列描述正確的是( )| A. | 反應開始到10s,用Z表示的反應速率為0.158mol/(L•s) | |
| B. | 反應開始到10s,X的物質的量濃度減少了0.79mol/L | |
| C. | 反應的化學方程式為:X(g)+Y(g)?Z(g) | |
| D. | 反應開始到10s時,Y的轉化率為79.0% |
分析 根據圖象知,隨著反應的進行,X、Y的物質的量減小,Z的物質的量增加,說明X、Y是反應物,Z是生成物,達到平衡時△n(X)=(1.20-0.41)mol=0.79mol,△n(Y)=(1.00-0.21)mol=0.79mol,△n(Z)=(1.58-0)mol=1.58mol,同一反應中同一時間段內各物質的物質的量變化之比等于其計量數之比,所以
X、Y、Z的計量數之比=1:1:1,則該反應方程式為X(g)+Y(g)?2Z(g),
A.反應開始到10s,用Z表示的反應速率=$\frac{△c}{△t}$=$\frac{\frac{△n}{V}}{△t}$;
B.反應開始到10s,X的物質的量濃度減少了 $\frac{0.79mol}{2L}$;
C.同一反應方程式中同一時間段內各物質的物質的量變化之比等于其計量數之比;
D.反應開始到10s時,Y轉化了(1.00-0.21)mol.
解答 解:根據圖象知,隨著反應的進行,X、Y的物質的量減小,Z的物質的量增加,說明X、Y是反應物,Z是生成物,達到平衡時△n(X)=(1.20-0.41)mol=0.79mol,△n(Y)=(1.00-0.21)mol=0.79mol,△n(Z)=(1.58-0)mol=1.58mol,同一反應中同一時間段內各物質的物質的量變化之比等于其計量數之比,所以
X、Y、Z的計量數之比=1:1:1,則該反應方程式為X(g)+Y(g)?2Z(g),
A.反應開始到10s,用Z表示的反應速率=$\frac{△c}{△t}$=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{1.58mol}{2L}}{10s}$=0.079mol/(L•s),故A錯誤;
B.反應開始到10s,X的物質的量濃度減少了 $\frac{0.79mol}{2L}$=0.395mol/L,故B錯誤;
C.通過以上分析知,該反應方程式為X(g)+Y(g)?2Z(g),故C錯誤;
D.反應開始到10s時,Y轉化了(1.00-0.21)mol=0.79mol,故D正確;
故選D.
點評 本題考查圖象分析,涉及方程式的確定、物質的量及物質的量濃度和反應速率的計算,熟練掌握基本公式及方程式中物質的量變化量與計量數的關系,題目難度不大.


 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源: 題型:實驗題
| 2min | 4min | 6nin | 8min | … | |
| CO | 0.07 | 0.06 | 0.06 | 0.05 | … |
| H2 | x | 0.12 | 0.12 | 0.20 | … |
| CH2OH | 0.03 | 0.04 | 0.04 | 0.05 | … |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2的電子式: | B. | S2-的結構示意圖: | ||
| C. | HF的電子式: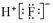 | D. | 肼(N2H4)的結構簡式:H2N-NH2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
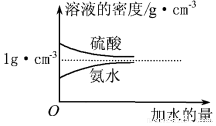
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 高溫下用焦炭還原SiO2制取粗硅 | |
| B. | 晶體硅熔點高硬度大,因此可用于制作半導體材料 | |
| C. | 石英只能用于生產光導纖維 | |
| D. | 玻璃容器可長期盛放各種酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | RCl | B. | RCl2 | C. | RCl3 | D. | RCl4 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com