
| A. | K2CO3和KCl | B. | NaCl和Na2CO3 | C. | NaCl和MgCl2 | D. | NaCl和KCl |
分析 只能用焰色反應進行鑒別,則選項中物質不能利用陰離子鑒別,且陽離子不同,陽離子利用化學反應不能鑒別,以此來解答.
解答 解:A.利用鹽酸可鑒別,加鹽酸生成無色氣體的為碳酸鉀,無現象的為氯化鉀,故A不選;
B.可加入鹽酸鑒別,碳酸鈉生成二氧化碳氣體,氯化鈉無現象,故B不選;
C.可加入氫氧化鈉溶液鑒別,氯化鎂生成沉淀,故C不選;
D.陰離子均為氯離子,只能利用焰色反應檢驗,焰色為黃色的為氯化鈉,則另一物質為氯化鉀,故D選.
故選D.
點評 本題考查物質的鑒別,為高頻考點,把握物質的性質、反應中的不同現象為解答的關鍵,注意焰色反應為物理變化,明確常見金屬的焰色反應即可解答,題目難度不大.


科目:高中化學 來源: 題型:實驗題
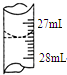 欲測定某NaOHmol•L-1溶液的物質的量濃度,可用0.100的HCl標準溶液進行中和滴定(用甲基橙作指示劑).
欲測定某NaOHmol•L-1溶液的物質的量濃度,可用0.100的HCl標準溶液進行中和滴定(用甲基橙作指示劑).| 實驗序號 | 待測NaOH溶液的體積/mL | 0.1000mol•L-1HCl溶液的體積/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4 L H2和Cl2的混合氣體中含有的分子數為2NA | |
| B. | 在標準狀況下,1 mol H2O的體積可能是22.4 L | |
| C. | 當溫度高于0℃時,一定量任何氣體的體積都大于22.4 L | |
| D. | 標況下,某氣體的體積為22.4 L,則該氣體的物質的量為1 mol,所含的分子數目約為:6.02×1023 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 假說經過反復驗證和修正,才發展成為科學的理論 | |
| B. | 研究物質的性質常用觀察、實驗、分類、比較等方法 | |
| C. | 在研究原子結構的過程中建立起的各種模型屬于思維模型 | |
| D. | 依據丁達爾現象可將分散系分為溶液、膠體與濁液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHCO3=Na++H++CO32- | B. | NH4NO3=NH4++NO3- | ||
| C. | NaHSO4=Na++H++SO42- | D. | Ba(OH)2=Ba2++2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
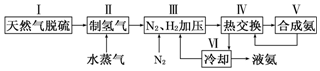
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com