
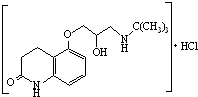
 )可用于治療心絞痛和青光眼.
)可用于治療心絞痛和青光眼.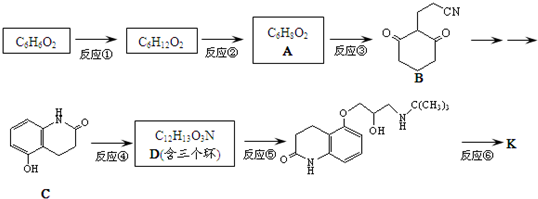
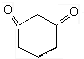 D
D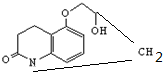
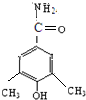
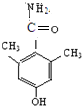 、
、
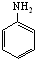 )與HNO2和H3PO2反應可得苯.請設計從C合成
)與HNO2和H3PO2反應可得苯.請設計從C合成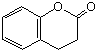 的路線.(合成路線常用的表示方法為:A$→_{反應條件}^{反應試劑}$B…$→_{反應條件}^{反應試劑}$目標產物)
的路線.(合成路線常用的表示方法為:A$→_{反應條件}^{反應試劑}$B…$→_{反應條件}^{反應試劑}$目標產物) 分析 根據A的分子式C6H8O2和B的結構簡式可知:A為: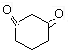 ,反應②C6H12O2→C6H8O2,為醇的催化氧化,反應為:
,反應②C6H12O2→C6H8O2,為醇的催化氧化,反應為: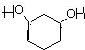 +O2$→_{△}^{Cu/Ag}$$→_{△}^{Cu/Ag}$
+O2$→_{△}^{Cu/Ag}$$→_{△}^{Cu/Ag}$ +2H2O,反應①C6H6O2→C6H12O2,為與氫氣的加成反應,反應為:
+2H2O,反應①C6H6O2→C6H12O2,為與氫氣的加成反應,反應為: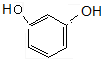 +3H2$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$
+3H2$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$ ,對照C和反應⑤后的產物,反應④為
,對照C和反應⑤后的產物,反應④為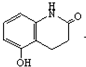 +HOCH2CH(OH)CH2OH→
+HOCH2CH(OH)CH2OH→ +H2O,反應⑤為:
+H2O,反應⑤為: +H2NC(CH3)3→
+H2NC(CH3)3→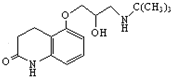 ,
, 和鹽酸反應得到K,
和鹽酸反應得到K,
苯胺( )與HNO2和H3PO2反應可得苯,
)與HNO2和H3PO2反應可得苯, 合成
合成 ,可先
,可先 水解開環得
水解開環得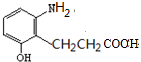 ,與HNO2和H3PO2反應可得
,與HNO2和H3PO2反應可得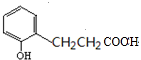 ,
,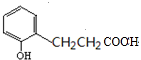 發生分子內脫水可得:
發生分子內脫水可得: .
.
解答 解:(1)反應①C6H6O2→C6H12O2,為C6H6O2與氫氣的加成反應,反應為: +3H2$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$
+3H2$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$$→_{△}^{催化劑}$ ,對照C和反應⑤后的產物,反應④為
,對照C和反應⑤后的產物,反應④為 +HOCH2CH(OH)CH2OH→
+HOCH2CH(OH)CH2OH→ +H2O,為取代反應,
+H2O,為取代反應,
故答案為:加成反應;取代反應;
(2)反應②C6H12O2→C6H8O2,為醇的催化氧化,反應為: +O2$→_{△}^{Cu/Ag}$$→_{△}^{Cu/Ag}$
+O2$→_{△}^{Cu/Ag}$$→_{△}^{Cu/Ag}$ +2H2O,反應⑤總反應為:
+2H2O,反應⑤總反應為: +H2NC(CH3)3→
+H2NC(CH3)3→ ,實質為
,實質為 在稀酸條件下的水解開環,
在稀酸條件下的水解開環, +H2O$→_{△}^{稀酸}$
+H2O$→_{△}^{稀酸}$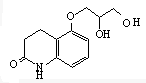 ,然后與H2NC(CH3)3發生縮合反應,
,然后與H2NC(CH3)3發生縮合反應,
故答案為:Cu/Ag;稀酸;
(3)根據A的分子式C6H8O2和B的結構簡式可知:A為: ,對照C和反應⑤后的產物,反應④為
,對照C和反應⑤后的產物,反應④為 +HOCH2CH(OH)CH2OH→
+HOCH2CH(OH)CH2OH→ +H2O,D為:
+H2O,D為: ,
,
故答案為: ;
; ;
;
(4)B的分子式為C9H11NO2,(1)能與Na2CO3溶液反應為酚羥基或羧基;(2)有兩種含氧官能團只能為羰基與羥基;(3)分子中有4種不同化學環境的氫原子,說明有四種氫原子,所以滿足以上條件的B的同分異構體的結構簡式為: 、
、 ,
,
故答案為: 、
、 ;
;
(5) 合成
合成 ,可先
,可先 水解開環得
水解開環得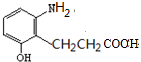 ,與HNO2和H3PO2反應可得
,與HNO2和H3PO2反應可得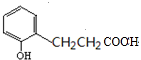 ,
,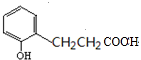 發生分子內脫水可得:
發生分子內脫水可得: ,所以合成的路線為:
,所以合成的路線為: →
→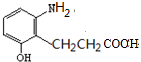 →
→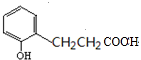 →
→ ,
,
故答案為: →
→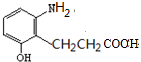 →
→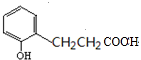 →
→ .
.
點評 本題考查有機物推斷,關鍵是熟練掌握官能團的性質與轉化,再結合反應條件利用題中信息及各物質轉化的條件進行物質結構的推斷,注意C→D推斷根據氨基、羥基的性質推斷為該題的難點,題目難度中等.


 名校通行證有效作業系列答案
名校通行證有效作業系列答案科目:高中化學 來源: 題型:選擇題
| A. | 石油裂解的目的是獲得更多的輕質液體燃料 | |
| B. | 石油裂化主要是得到乙烯、丙烯等小分子烴 | |
| C. | 石油分餾是物理變化,可分離得到汽油、柴油、煤油等多種餾分,它們都是純凈物 | |
| D. | 煤的干餾是化學變化,可從得到的煤焦油中提取苯,甲苯等重要的化工原料 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
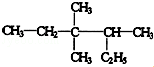 3,3,4-三甲基已烷分子結構中有1個手性碳原子.
3,3,4-三甲基已烷分子結構中有1個手性碳原子. ,
,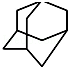 的分子式為C10H16,1mol該烴完全燃燒,需要標準狀況下氧氣313.6升.
的分子式為C10H16,1mol該烴完全燃燒,需要標準狀況下氧氣313.6升.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何氧化還原反應原則上都可以設計成原電池 | |
| B. | 原電池中電子從負極經導線流入正極 | |
| C. | 原電池中正極得電子數與負極失電子數一定相等 | |
| D. | 銅-鋅-稀硫酸組成的原電池,電解質溶液中H+向負極移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X的I1大于Y 的I1 | B. | X的電負性小于Y的電負性 | ||
| C. | X的陰離子半徑小于Y的陽離子半徑 | D. | X的原子半徑大于Y的原子半徑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l)△H1=aKJ•mol-1 | |
| B. | HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l)△H2=bKJ•mol-1 | |
| C. | HCl(aq)+NH3•H2O (aq)=NH4Cl(aq)+H2O(l)△H3=cKJ•mol-1 | |
| D. | H+(aq)+OH-(aq)+$\frac{1}{2}$Ba2+(aq)+$\frac{1}{2}$SO42-(aq)=$\frac{1}{2}$BaSO4(s)+H2O(l)△H4=dKJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化銀為正極,被氧化 | |
| B. | 負極發生的反應為:Zn+2OH--2e-═ZnO+H2O | |
| C. | Zn為負極,被還原 | |
| D. | 該裝置中的電解質為酸性物質 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com