
| 溫度/°C | K1 | K2 |
| 500 | 1.00 | 3.5 |
| 700 | 1.47 | 2.26 |
| 900 | 2.40 | 1.60 |
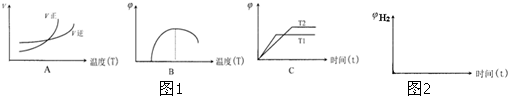
| 1 |
| 2 |
| 2mol/L-1mol/L |
| 2mol/L |
 ,
, .
.


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案科目:高中化學 來源: 題型:
| A、甲苯、氯仿、己烯、酒精、苯酚水溶液、純堿 |
| B、五瓶無色溶液:乙醇、乙醛、乙酸、葡萄糖、丙三醇 |
| C、四瓶無色液體:己烯、環己烷、溴乙烷、苯 |
| D、四瓶無色溶液:CCl4、苯乙烯、乙醇、苯酚溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:
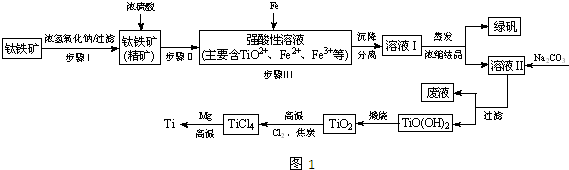
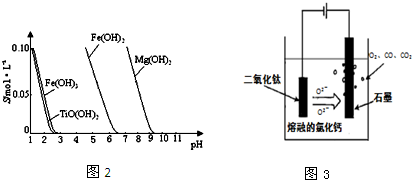
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔點/℃ | -25.0 | 648.8 | 714 | 1667 |
| 沸點/℃ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、Fe3+、Cu2+ |
| B、Fe2+、Cu2+ |
| C、Fe2+、Fe3+ |
| D、Fe3+、Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
| A、m+n>p |
| B、C的體積分數增加 |
| C、平衡向正反應方向移動 |
| D、A 的轉化率降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 某同學想利用鎂與鹽酸或醋酸在不同溫度下反應,探究外界條件對反應速率的影響.部分實驗用表如下:
某同學想利用鎂與鹽酸或醋酸在不同溫度下反應,探究外界條件對反應速率的影響.部分實驗用表如下:| 實驗 編號 | 溫度/K | 鹽酸濃度 /mol?L-1 | 醋酸濃度/mol?L-1 | 實驗目的 |
| ① | 298 | 0.20 | a.實驗①和②,探究溫度對反應速率的影響; b.實驗①和③,探究濃度對反應速率的影響; c.實驗④⑤,探究溫度對鎂與鹽酸反應和鎂與醋酸反應速率的影響,哪個更大一些. | |
| ② | 308 | 0.20 | ||
| ③ | 298 | 0.40 | ||
| ④ | 0.20 | |||
| ⑤ | 0.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、6mol C+2mol D |
| B、1mol A+0.5mol B+1.5mol C+0.5mol D |
| C、1mol A+0.5mol B+1.5mol C |
| D、4mol A+2mol B |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com