
分析 1.00g N2H4(1)與足量N2O4(l)完全反應生成N2(g)和H2O(l),放出19.14kJ的熱量,則1molN2H4(1)與足量N2O4(l)完全反應生成N2(g)和H2O(l),放出的熱量為19.14kJ×32=612.48kJ,結合物質的量與反應放出的熱量成正比計算.
解答 解:1.00g N2H4(1)與足量N2O4(l)完全反應生成N2(g)和H2O(l),放出19.14kJ的熱量,則1molN2H4(1)與足量N2O4(l)完全反應生成N2(g)和H2O(l),放出的熱量為19.14kJ×32=612.48kJ,可知2N2H4(l)+N2O4(l)═3N2(g)+4H2O(l)的△H=-1224.96kJ•mol-1,
故答案為:-1224.96.
點評 本題考查反應熱與焓變,為高頻考點,把握物質的量與反應中熱量變化成正比為解答的關鍵,側重分析與計算能力的考查,注意放熱時焓變為負,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:實驗題
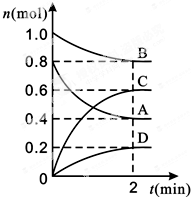 T℃時,在容積為0.5L的密閉容器中發生某一反應,且測得不同時間容器中四種物質A、B、C、D的物質的量變化如圖所示.已知:物質A、B、C均為氣態、D為固態,正反應是吸熱反應.根據要求回答下列問題:
T℃時,在容積為0.5L的密閉容器中發生某一反應,且測得不同時間容器中四種物質A、B、C、D的物質的量變化如圖所示.已知:物質A、B、C均為氣態、D為固態,正反應是吸熱反應.根據要求回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 有A、B、C、D、E、F六種短周期元素,其元素特征信息如表:
有A、B、C、D、E、F六種短周期元素,其元素特征信息如表:| 元素編號 | 元素特征信息 |
| A | A的單質是密度最小的物質 |
| B | B的單質能與冷水劇烈反應,所得強堿性溶液中含有兩種電子數相同的陰、陽離子 |
| C | C的原子最外層電子數是其內層電子數的三倍 |
| D | D與B同周期,該周期中D的簡單離子半徑最小 |
| E | B、C、E組成的36電子的化合物Y是家用消毒劑的主要成分 |
| F | F元素最高正價與最低負價的代數和為4 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
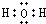 和
和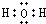 .
.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 A、B、C、D、E五種短周期元素,它們的原子序數依次增大;A元素的原子半徑最小;B元素的最高價氧化物對應水化物與其氫化物能生成鹽;D與A同主族,且與E同周期;E元素原子的最外層電子數比次外層電子數少2;A、B、D、E這四種元素,每一種與C元素都能形成原子個數比不相同的若干種化合物.請回答:
A、B、C、D、E五種短周期元素,它們的原子序數依次增大;A元素的原子半徑最小;B元素的最高價氧化物對應水化物與其氫化物能生成鹽;D與A同主族,且與E同周期;E元素原子的最外層電子數比次外層電子數少2;A、B、D、E這四種元素,每一種與C元素都能形成原子個數比不相同的若干種化合物.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 熱穩定性:HF<HCl<HBr<HI | B. | 微粒半徑:Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 還原性:Na<Mg<Al |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com