

| n |
| V |
| n |
| V |


 名題金卷系列答案
名題金卷系列答案 優加精卷系列答案
優加精卷系列答案科目:高中化學 來源: 題型:
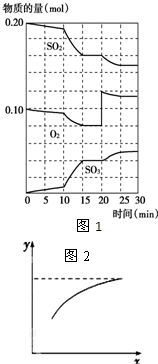 硫酸生產中,接觸室內的反應為:
硫酸生產中,接觸室內的反應為:
| ||
| △ |
| X | y | |
| A | 再加入SO2 | O2的轉化率 |
| B | 再加入SO3 | SO2的體積分數 |
| C | 壓強 | 混合氣體的物質的量 |
| D | 溫度 | 混合氣體的平均摩爾質量 |
| 容器 | 甲 | 乙 | 丙 | 丁 |
| 起始投入量 | 2mol SO2+ 1mol O2 | 1mol SO2+ 0.5mol O2 | 2mol SO3 | 2mol SO2+ 2mol O2 |
| 反應放出或 吸收的熱量(kJ) | a | b | c | d |
| 平衡時c(SO3)(mol/L) | e | f | g | h |
查看答案和解析>>
科目:高中化學 來源: 題型:
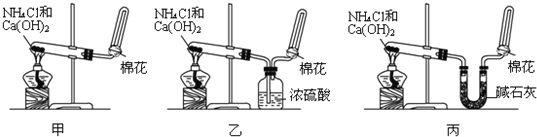
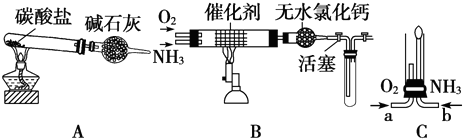
查看答案和解析>>
科目:高中化學 來源: 題型:
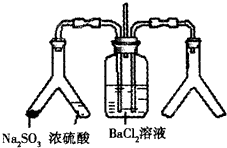 將SO2通入BaCl2溶液并不產生沉淀,而通入另一種氣體后可以產生白色沉淀.則右側Y形管中放置的藥品組合不符合要求的是(必要時可以加熱)( )
將SO2通入BaCl2溶液并不產生沉淀,而通入另一種氣體后可以產生白色沉淀.則右側Y形管中放置的藥品組合不符合要求的是(必要時可以加熱)( )| A、石灰石和稀硝酸 |
| B、CaO和氯化銨 |
| C、Cu和濃硝酸 |
| D、Na2O2和食鹽水 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
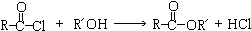
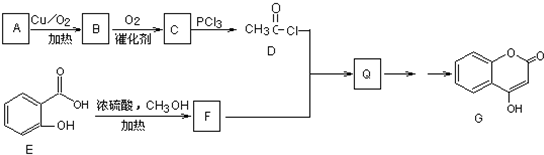
查看答案和解析>>
科目:高中化學 來源: 題型:
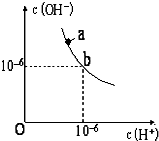 回答下列問題.
回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:
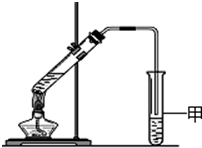 通過糧食發酵可獲得某含氧有機物X,其相對分子質量為46,其中碳的質量分數為52.2%,氫的質量分數為13.0%.
通過糧食發酵可獲得某含氧有機物X,其相對分子質量為46,其中碳的質量分數為52.2%,氫的質量分數為13.0%.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com