
分析 (1)純堿為碳酸鈉,屬于強堿弱酸鹽水解溶液呈堿性;
(2)泡沫滅火器裝有碳酸氫鈉溶液和硫酸鋁溶液發生雙水解生成氫氧化鋁和二氧化碳;
(3)難溶電解質之間可實現由溶度積常數較大的物質轉化為溶度積常數較小的物質,Ksp(AgCl)>Ksp(AgI),白色沉淀為AgCl,黃色沉淀為AgI.
解答 解:(1)Na2CO3溶液中存在水解離子反應為:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,溶液呈堿性,
故答案為:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-;
(2)泡沫滅火器裝有碳酸氫鈉溶液和硫酸鋁溶液,碳酸氫鈉屬于強堿弱酸鹽的酸式鹽,硫酸鋁屬于強酸弱堿鹽,兩者發生雙水解,所以泡沫滅火器的反應原理為:Al3++3HCO3-=Al(OH)3↓+3CO2↑,
故答案為:Al3++3HCO3-=Al(OH)3↓+3CO2↑.
(3)難溶電解質之間可實現由溶度積常數較大的物質轉化為溶度積常數較小的物質,AgCl的濁液中加入KI溶液,白色沉淀AgCl變為黃色沉淀AgI,離子反應為AgCl+I-?AgI+Cl-.,
故答案為:AgCl+I-?AgI+Cl-.
點評 本題考查了離子方程式的書寫,題目難度不大,熟悉反應的實質是解題關鍵,注意雙水解徹底的用等號.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe3+、NH4+、SCN-、Cl- | B. | K+、Na+、SO42-、HCO3- | ||
| C. | Na+、Ba2+、Cl-、NO3- | D. | A13+、Na+、A1O2-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2Fe+4H2O═Fe2O3+4H2 | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | Ca(OH)2+SO2═CaSO3+H2O | D. | Cu+2H2SO4(濃)═CuSO4+SO2↑+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
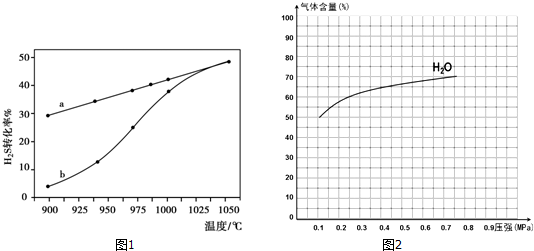
| 流程1:氣化爐中產生H2 | 流程2:燃燒爐中CaO再生 |
| 通入水蒸氣,主要化學反應: Ⅰ:C(s)+H2O(g)═CO(g)+H2(g) K1 Ⅱ:CO(g)+H2O(g)═CO2(g)+H2(g)K2 Ⅲ:CaO(s)+CO2(g)═CaCO3(s)K3 | 通入純氧,主要化學反應: IV:C(s)+O2(g)═CO2(g) △H=-393.8kJ•mol-1 V:CaCO3(s)═CaO(s)+CO2(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 由①可推測溶液中一定含大量CO32-、S2-、SO32-、NO3- | |
| B. | 由②可推測溶液中一定含大量NO2- | |
| C. | 由③可推測溶液中一定含大量NO3- | |
| D. | 由實驗④難以推測溶液中一定含大量SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com