
| A. | 聚乙烯食品包裝袋、食物保鮮膜都是無毒的高分子化合物 | |
| B. | 高純度的二氧化硅廣泛用于制作光導纖維,遇強堿會“斷路” | |
| C. | 煤經過氣化和液化兩種物理變化,可變為清潔能源 | |
| D. | 加熱能殺死甲型H1N1流感病毒,主要是加熱后使病毒中的蛋白質變性 |
分析 A.聚乙烯是無毒的高分子化合物;
B.高純度的二氧化硅廣泛用于制作光導纖維,二氧化硅能夠和強堿溶液反應;
C.煤的氣化和液化是化學變化;
D.加熱能使蛋白質變性.
解答 解:A.聚乙烯是無毒的高分子化合物,可制作食品包裝袋、食物保鮮膜,故A正確;
B.二氧化硅能夠和強堿溶液反應,光導纖維遇強堿會“斷路”,高純度的二氧化硅廣泛用于制作光導纖維,故B正確;
C.煤的氣化是煤與水蒸汽反應H2、CO等氣體的過程.煤的液化是將煤與H2在催化劑作用下轉化為液體燃料或利用煤產生的H2和CO通過化學合成產生液體燃料或其他液體化工產品的過程,兩種過程都生成了新物質,是化學變化,故C錯誤;
D.病毒的成分是蛋白質,加熱能使蛋白質變性,故D正確.
故選C.
點評 本題考查聚乙烯、蛋白質的變性、煤的氣化和液化、光導纖維等,比較基礎,側重對基礎知識的鞏固,注意對基礎知識的理解掌握.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 都能使溴水和酸性高錳酸鉀溶液褪色 | |
| B. | 都能發生加聚反應生成高分子化合物 | |
| C. | 都不溶于水,且密度比水小 | |
| D. | 分子中各原子都處于同一平面上 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1L0.1mol/L的NaHCO3溶液中HCO3-和CO3 2-離子數之和為0.1NA | |
| B. | 標準狀況下,22.4LC2H4與C3H6混合氣體所含有分子數為NA | |
| C. | 1molNa2O2與足量的CO2反應轉移的電子數為2NA | |
| D. | 18gNH4+所含的電子數11NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| Cu(OH)2 | Mg(OH)2 | Fe(OH)3 | Al(OH)3 | |
| 開始沉淀的pH | 4.8 | 9.3 | 2.7 | 3.8 |
| 完全沉淀的pH | 6.4 | 10.8 | 3.7 | 4.7 |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 測定次數 | 鹽酸的體積/mL | KOH溶液的體積 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 這類電池的正極反應與金屬的吸氧腐蝕正極反應相似 | |
| B. | 每轉移1mol電子則這種電池產生電能為0.5度電 | |
| C. | 電池的負極反應為:CH4+10OH-═CO32-+7H2O+8e- | |
| D. | 當消耗0.4mol燃料時,電池中的各種離子的濃度關系為:C(K+)>C(HCO3-)>C(CO32-)>C(OH-)>C(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.4g乙烯與丙烯的混合氣體含有NA個碳原子 | |
| B. | 精煉銅,若陽極失去2NA個電子,則陰極增重64g | |
| C. | 在1L 0.1mol/L的Na2CO3溶液中,陰離子總數小于0.1NA | |
| D. | 將1L 2mol/L的FeCl3溶液加入到沸水中,加熱使之完全反應,所得氫氧化鐵膠體粒子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
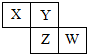
| A. | W的原子序數不可能是X的原子序數的3倍 | |
| B. | Z元素可能是金屬元素 | |
| C. | W的氣態氫化物的穩定性一定比Y的強 | |
| D. | 四種元素的原子有可能均能與氫原子形成18電子分子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com