
| A. | ①②③ | B. | ①②④ | C. | ②③④ | D. | ①③④ |
分析 ①常溫在c(H+)/c(OH-)=10-10溶液中存在大量氫氧根離子,四種離子之間不反應,都不與氫氧根離子反應;
②常溫pH=11的溶液中存在大量氫氧根離子,四種離子之間不反應,都不與氫氧根離子反應;
③水電離出的H+濃度c(H+)=10-12mol•L?1的溶液中存在大量氫離子或氫氧根離子,S2O32-與與氫離子反應,酸性條件下硝酸根離子能夠氧化S2O32-;
④使甲基橙變紅色的溶液中存在大量氫離子,四種離子之間不反應,都不與氫離子反應.
解答 解:①常溫在c(H+)/c(OH-)=10-10溶液呈堿性,K+、Na+、CH3COO-、SO42-之間不反應,都不與氫氧根離子反應,在溶液中能夠大量共存,故①正確;
②常溫pH=11的溶液呈堿性,溶液中存在大量氫氧根離子,CO32-、Na+、AlO2-、NO3-之間不發生反應,都不與氫氧根離子反應,在溶液中能夠大量共存,故②正確;
③水電離出的H+濃度c(H+)=10-12mol•L?1的溶液呈酸性或堿性,NO3-、S2O32-在酸性條件下發生氧化還原反應,在酸性溶液中不能大量共存,故③錯誤;
④使甲基橙變紅色的溶液呈酸性,溶液中存在大量氫離子,Fe3+、NO3-、Na+、SO42-之間不反應,都不與氫離子反應,在溶液中能夠大量共存,故④正確;
故選B.
點評 本題考查離子共存的判斷,題目難度不大,注意明確離子不能大量共存的一般情況:能發生復分解反應的離子之間;能發生氧化還原反應的離子之間;等;還應該注意題目所隱含的條件,如:溶液的酸堿性,據此來判斷溶液中是否有大量的 H+或OH-;溶液的顏色,如無色時可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色離子的存在;溶液的具體反應條件,如“氧化還原反應”、“加入鋁粉產生氫氣”;是“可能”共存,還是“一定”共存等;試題側重對學生基礎知識的訓練和檢驗,有利于培養學生的邏輯推理能力,提高學生靈活運用基礎知識解決實際問題的能力.


科目:高中化學 來源: 題型:多選題
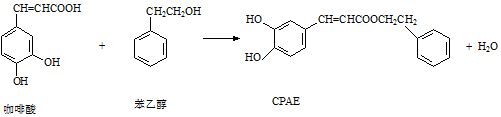
| A. | 苯乙醇屬于芳香醇,它與鄰甲基苯酚互為同系物 | |
| B. | 1 mol CPAE最多可與含3 mol NaOH的溶液發生反應 | |
| C. | 不能用FeCl3溶液可以檢測上述反應中是否有CPAE生成 | |
| D. | 咖啡酸、苯乙醇及CPAE都能發生取代、加成和消去反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

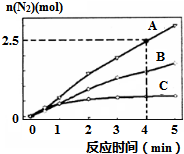
| 編號 | 反應溫度/℃ | Na2S2O3濃液/mL | 甲 | 0.1mol/LH2SO4溶液/mL | 乙 |
| ① | 25℃ | 10.0 | 0 | 10.0 | |
| ② | 25℃ | 5.0 | a | 10.0 | |
| ③ | 45℃ | 10.0 | 0 | 10.0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 中和時所需NaOH的量 | B. | 與Mg反應的起始速率 | ||
| C. | OH-的物質的量濃度 | D. | 溶液中$\frac{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 化學式 | 電離常數(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 氨在生活、生產、科研中有廣泛用途.
氨在生活、生產、科研中有廣泛用途.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
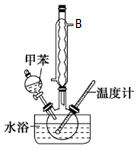 硝基甲苯有領、間、對三種,其中對硝基甲苯是醫藥、染料等工業的一種重要有機中間體,它常以濃硝酸為硝化劑,濃硫酸為催化劑,通過甲苯的硝化反應制備.一種新的制備對硝基甲苯的實驗方法是:以發煙硝酸為硝化劑,固體NaHSO4為催化劑(可循環使用),在CCl4溶液中,加入乙酸酐(有脫水作用),45℃反應1h.反應結束后,過濾,濾液分別用5%NaHCO3,溶液、水洗至中性,再經分離提純得到對硝基甲苯.
硝基甲苯有領、間、對三種,其中對硝基甲苯是醫藥、染料等工業的一種重要有機中間體,它常以濃硝酸為硝化劑,濃硫酸為催化劑,通過甲苯的硝化反應制備.一種新的制備對硝基甲苯的實驗方法是:以發煙硝酸為硝化劑,固體NaHSO4為催化劑(可循環使用),在CCl4溶液中,加入乙酸酐(有脫水作用),45℃反應1h.反應結束后,過濾,濾液分別用5%NaHCO3,溶液、水洗至中性,再經分離提純得到對硝基甲苯.| 催化劑 | n(催化劑) | 硝化產物中各種異構體質量分數(%) | 總產率 (%) | ||
| n(甲苯) | 對硝基甲苯 | 鄰硝基甲苯 | 間硝基甲苯 | ||
| 濃H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 82.0 |
| 1.2 | 36.5 | 59.2 | 4.0 | 83.8 | |
NaHSO4 | 0.25 | 46.3 | 52.8 | 0.9 | 92.8 |
| 0.32 | 48.0 | 51.7 | 0.3 | 95.0 | |
| 0.36 | 45.0 | 54.4 | 0.6 | 93.9 | |
| 密度/g•cm-3 | 沸點/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 對硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液態烴 |
| 鄰硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液態烴 |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化劑和還原劑物質的量之比為5:4 | |
| B. | 3 mol H2S可還原4mol的KIO3 | |
| C. | I2是還原產物,K2SO4是氧化產物 | |
| D. | 1molKIO3可氧化0.2mol的KI |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com