
| A. | 某溶液中滴加AgNO3溶液有白色沉淀,說明原溶液中有Cl- | |
| B. | 某溶液中先滴足量鹽酸無現象,再滴加BaCl2溶液有白色沉淀,說明原溶液中有SO42- | |
| C. | 某溶液中滴加NaOH溶液有藍色沉淀,說明原溶液中有Fe3+ | |
| D. | 某溶液中滴加稀硫酸生成無色氣體,說明原溶液中有CO32- |
分析 A.白色沉淀可能為AgCl或硫酸銀等;
B.先滴足量鹽酸無現象,排除干擾離子,再滴加BaCl2溶液有白色沉淀,則白色沉淀為硫酸鋇;
C.滴加NaOH溶液有藍色沉淀,沉淀為氫氧化銅;
D.無色氣體為二氧化碳或二氧化硫.
解答 解:A.白色沉淀可能為AgCl或硫酸銀等,則原溶液中可能有Cl-或SO42-,故A不選;
B.先滴足量鹽酸無現象,排除干擾離子,再滴加BaCl2溶液有白色沉淀,則白色沉淀為硫酸鋇,則原溶液中有SO42-,故B選;
C.滴加NaOH溶液有藍色沉淀,沉淀為氫氧化銅,則溶液中含Cu2+,故C不選;
D.無色氣體為二氧化碳或二氧化硫,則原溶液中有CO32-或HCO3-,或SO32-等,故D不選;
故選B.
點評 本題考查常見離子的檢驗,為高頻考點,把握離子檢驗的試劑、現象與結論為解答的關鍵,側重分析與實驗能力的考查,注意排除干擾離子,題目難度不大.


 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案 綜合自測系列答案
綜合自測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 電離平衡常數可以表示弱電解質的相對強弱 | |
| B. | 電離平衡常數受溶液濃度的影響 | |
| C. | H2CO3的電離常數表達式:K=$\frac{c({H}^{+})•c(C{O}_{3}^{2-})}{c({H}_{2}C{O}_{3})}$ | |
| D. | 電離常數大的酸溶液中c(H+)一定比電離常數小的酸中大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ⑥⑤②①④③ | B. | ⑤⑥②①③④ | C. | ④③②①⑤⑥ | D. | ④③①②⑥⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{{{r}_{N{a}^{+}}}^{\;}}{{r}_{Na}}$ | B. | $\frac{{r}_{Mg}}{{r}_{Na}}$ | C. | $\frac{{r}_{p}}{{r}_{Cl}}$ | D. | $\frac{{r}_{N}}{{r}_{p}}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
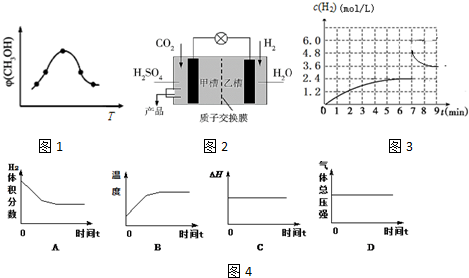
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 保持溫度和活塞位置不變,在甲中再加入1 mol A和2 mol B,達到新的平衡后,甲中C的濃度是乙中C的濃度的2倍 | |
| B. | 保持活塞位置不變,升高溫度,達到新的平衡后,甲、乙中B的體積分數均減少 | |
| C. | 保持溫度和乙中的壓強不變,t2時分別向甲、乙中加入等質量的氦氣后,甲、乙中反應速率變化情況分別如圖2和圖3所示(t1前的反應速率變化已省略) | |
| D. | 保持溫度不變,移動活塞P,使乙的容積和甲相等,達到新的平衡后,乙中C的體積分數是甲中C 的體積分數的2倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Ba2+、S2-、SO42- | B. | Na+、Cu2+、SO42-、Cl- | ||
| C. | Br-、Ba2+、Cl-、K+ | D. | Ca2+、K+、CO32-、NO3- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com