
分析 鋅與濃硫酸發生:Zn+2H2SO4=ZnSO4+SO2↑+H2O,隨著反應的進行,硫酸濃度降低,發生:Zn+H2SO4=ZnSO4+H2↑,生成氣體為SO2和H2的混合物,物質的量為:$\frac{33.6L}{22.4L/mol}$=1.5mol,剩余硫酸的物質的量為:n(H2SO4)剩=$\frac{1}{2}$×1L×0.1mol/L=0.05mol,消耗硫酸的物質的量為:n(H2SO4)消耗=0.1L×18.5mol/L-0.05mol=1.8mol,根據反應的化學方程式計算.
解答 解:n(H2SO4)濃=0.1L×18.5mol/L=1.85mol,
剩余硫酸的物質的量為:n(H2SO4)剩=$\frac{1}{2}$×1L×0.1mol/L=0.05mol,
消耗硫酸的物質的量為:n(H2SO4)消耗=1.85mol-0.05mol=1.8mol,
鋅與濃硫酸發生:Zn+2H2SO4=ZnSO4+SO2↑+H2O,隨著反應的進行,硫酸濃度降低,發生:Zn+H2SO4=ZnSO4+H2↑,
生成氣體為SO2和H2的混合物,物質的量為$\frac{33.6L}{22.4L/mol}$=1.5mol,
設混合物氣體中含有xmolSO2,ymolH2,
Zn+2H2SO4=ZnSO4+SO2↑+H2O
2xmol xmol
Zn+H2SO4=ZnSO4+H2↑
ymol ymol
則:$\left\{\begin{array}{l}{x+y=1.5}\\{2x+y=1.8}\end{array}\right.$
解得:$\left\{\begin{array}{l}{x=0.3}\\{y=1.2}\end{array}\right.$
則氣體A中n(SO2):n(H2)=x:y=0.3:1.2=1:4,
所以V(SO2):V(H2)=(0.3×224):(1.2×22.4)=1:4
答:氣體A中各組分的體積比V(SO2):V(H2)=1:4.
點評 本題考查化學方程式的計算,題目難度中等,本題注意以下幾點:①濃硫酸與鋅反應生成SO2,②隨著反應的進行,硫酸的濃度降低,與鋅反應生成H2,③根據反應的方程式利用守恒的方法列式計算.


科目:高中化學 來源: 題型:選擇題
| A. | Al3+、Na+、SO42-、Cl- | B. | Na+、K+、CO32-、SO42- | ||
| C. | K+、NH4+、Cl-、NO3- | D. | Na+、Ba2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
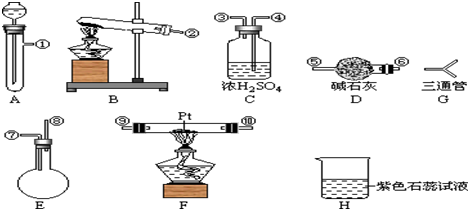
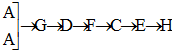 [按裝置先后順序排列]
[按裝置先后順序排列]查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電子云示意圖中的小黑點表示原子核最外層的電子 | |
| B. | 某元素有多種同位素,天然存在的該元素其中一種同位素的豐度為75%,則100 g天然存在的該元素中,此同位素的質量為75 g | |
| C. | 核外電子的運動狀態是由該電子的電子層、電子亞層、電子云的伸展方向和電子自旋方向共同決定的 | |
| D. | 電子離核越遠能量越高,所以N層電子的能量一定高于M層電子的能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 單質分子中一定存在共價鍵;最外層有2個電子的原子都是金屬原子 | |
| B. | 非極性鍵可以存在于離子化合物中; 質子數相同的粒子不一定屬于同種元素 | |
| C. | 同位素的化學性質幾乎完全相同;任何原子的原子核都是由質子和中子構成的 | |
| D. | PCl3和BCl3分子中所有原子的最外層都達到8電子穩定結構; 伴有能量變化的物質變化都是化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應除了生成新物質外,還伴隨著能量的變化 | |
| B. | 放熱反應可能需要加熱才可以發生 | |
| C. | 反應條件是加熱的反應都是吸熱反應 | |
| D. | 化學反應放熱還是吸熱,取決于生成物具有的總能量和反應物具有的總能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對于相同pH的弱酸HX和HY(前者的Ka較小),加水稀釋后pH值仍相同,則前者酸中稀釋的倍數更大 | |
| B. | 在CH3COOH和CH3COONa濃度均為0.1mol/L的體系中,外加少量強堿時,溶液的PH值發生較大變化 | |
| C. | 在Na2HPO4水溶液中存在關系式:c(H3PO4)+c(H2PO4-)+c(HPO42-)+c(PO43-)═c(Na+) | |
| D. | 沉淀溶解平衡BaSO4═Ba2++SO42- 的沉淀溶解平衡常數為1.1×10-10,說明難溶鹽BaSO4是弱電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃度均為0.1 mol•L-1的CH3COOH和CH3COONa溶液等體積混合所得的溶液中:c(CH3COOH)+c(CH3COO-)═0.2 mol•L-1 | |
| B. | 0.1 mol•L-1 NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 0.2 mol•L-1 HCl溶液與等體積0.1 mol•L-1 NaOH溶液混合后,溶液的pH=1 | |
| D. | 0.1 mol•L-1氨水中滴入0.1 mol•L-1鹽酸至溶液呈中性時:c(NH4+)=c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 點燃 | B. | 聞氣味 | ||
| C. | 濕潤的淀粉碘化鉀試紙 | D. | 干燥pH試紙 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com