
| 溶質 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 0.1 mol•L-1 Na2CO3溶液中,存在關系:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| B. | 加熱0.1 mol•L-1 NaClO溶液測其pH,pH小于9.7 | |
| C. | pH=2的HF溶液與pH=12的NaOH溶液以等體積混合,則有c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | 根據上表數據得出三種酸電離平衡常數大小關系為:HF>HClO>H2CO3(一級電離平衡常數) |
分析 A.根據物料守恒:2[c(CO32-)+c(HCO3-)+c(H2CO3)]=c(Na+),根據電荷守恒得c(H+)+c(Na+)=c(OH-)+c(HCO3-)+2c(CO32-);
B.鹽類水解是吸熱反應,升高溫度促進鹽類水解;
C.常溫下NaF溶液pH=7.5>7,NaF溶液呈堿性,說明NaF是強堿弱酸鹽,則HF是弱酸;pH=2的HF濃度大于pH=12的NaOH溶液濃度,二者等體積混合HF有剩余,溶液呈酸性;
D.相同溫度下,相同濃度的鈉鹽溶液中,弱酸根離子水解程度越大其溶液pH越大,酸根離子水解程度越大其相對應的酸的電離程度越小,即酸的電離平衡常數越小.
解答 解:A.A.根據物料守恒:2[c(CO32-)+c(HCO3-)+c(H2CO3)]=c(Na+),根據電荷守恒得c(H+)+c(Na+)=c(OH-)+c(HCO3-)+2c(CO32-),所以得c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3),故A正確;
B.鹽類水解是吸熱反應,升高溫度促進鹽類水解NaClO溶液pH>7,則NaClO是強堿弱酸鹽,升高溫度促進其水解,溶液的堿性增強,pH增大,故B錯誤;
C.常溫下NaF溶液pH=7.5>7,NaF溶液呈堿性,說明NaF是強堿弱酸鹽,則HF是弱酸;pH=2的HF濃度大于pH=12的NaOH溶液濃度,二者等體積混合HF有剩余,溶液呈酸性,則c(H+)>c(OH-),結合電荷守恒得c(Na+)<c(F-),酸的電離程度較小,則溶液中離子濃度大小順序是c(F-)>c(Na+)c(H+)>c(OH-),故C錯誤;
D.相同溫度下,相同濃度的鈉鹽溶液中,弱酸根離子水解程度越大其溶液pH越大,酸根離子水解程度越大其相對應的酸的電離程度越小,即酸的電離平衡常數越小,根據表中數據知,酸根離子水解程度F-<ClO-<CO32-,則酸的電離平衡常數HF>HClO>HCO3-,故D錯誤;
故選A.
點評 本題考查離子濃度大小比較,為高頻考點,側重考查學生分析推斷能力,明確酸的電離程度與酸根離子水解程度關系、溶液中溶質成分及其性質是解本題關鍵,易錯選項是D,注意碳酸根離子對應的酸是碳酸氫根離子而不是碳酸,題目難度不大.


 云南師大附小一線名師提優作業系列答案
云南師大附小一線名師提優作業系列答案 沖刺100分單元優化練考卷系列答案
沖刺100分單元優化練考卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 氨基鈉和氫化鈉與鹽酸反應都只生成一種鹽 | |
| B. | 方程式②中,每生成1mol H2轉移1 mol電子 | |
| C. | 熔融氫化鈉不導電 | |
| D. | 方程式①中,氨基鈉是還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
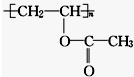
| A. | 1 mol 該有機物與 NaOH 溶液完全反應時,消耗 1 mol NaOH | |
| B. | 該有機物水解所得產物能發生酯化反應 | |
| C. | 該有機物可通過加聚反應生成 | |
| D. | 該有機物屬于混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 200mL 2mol/L蔗糖溶液中所含分子數為0.4NA | |
| B. | 標準狀況下,2.24L HF的氫原子數目為0.1 NA | |
| C. | 黑火藥爆炸的方程式為2KNO3+3C+S═K2S+N2↑+3CO2↑,當生成1molK2S時轉移電子數為2NA | |
| D. | 標準狀況下,1.12L 1H2和0.2g2H2均含有0.1 NA質子 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同分異構體之間分子式相同,其式量也一定相等;式量相等的物質一定是同分異構體 | |
| B. | 某有機物燃燒后產物只有CO2和H2O,可推出的結論是有機物屬于烴 | |
| C. | 分子式為C2H6O的紅外光譜圖上發現有C-H鍵和C-O鍵的振動吸收,由此可以初步推測有機物結構簡式為CH3CH2OH | |
| D. | 分子式為C8H10的芳香烴有4種同分異構體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com