
 某原電池裝置如圖所示,電池總反應為2Ag+Cl2=2AgCl.
某原電池裝置如圖所示,電池總反應為2Ag+Cl2=2AgCl.分析 根據電池總反應為2Ag+Cl2═2AgCl可知,Ag失電子作負極失電子,氯氣在正極上得電子生成氯離子,
(1)正極上氯氣得電子;
(2)放電時,交換膜左則的氫離子向正極移動,氯離子與銀離子生成氯化銀沉淀;
(3)根據電池總反應判斷.
解答 解:根據電池總反應為2Ag+Cl2═2AgCl可知,Ag失電子作負極失電子,氯氣在正極上得電子生成氯離子,
(1)正極上氯氣得電子生成氯離子,其電極反應為:Cl2+2e-═2Cl-,故答案為:Cl2+2e-═2Cl-;
、(2)放電時,交換膜左側溶液中生成銀離子,銀離子與氯離子反應生成氯化銀沉淀,所以交換膜左側溶液中有大量白色沉淀生成,
故答案為:交換膜左側溶液大量白色沉淀生成;
(3)放電時,當電路中轉移0.01mol e-時,交換膜左則會有0.01mol氫離子通過陽離子交換膜向正極移動,同時會有0.01molAg失去0.01mol電子生成銀離子,銀離子會與氯離子反應生成氯化銀沉淀,所以氯離子會減少0.01mol,則交換膜左側溶液中約減少0.02mol離子,
故答案為:0.02.
點評 本題考查了原電池原理的應用及沉淀反應,注意把握原電池原理及正負極的判斷和電極方程式的書寫,利用電子及電荷守恒來解決原電池中有關計算的問題,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 向Ba(NO3)2溶液中通入CO2不產生白色沉淀,則通入SO2也不產生白色沉淀 | |
| B. | 電負性:C<N<O,則第一電離能:C<N<O | |
| C. | 乙醛能被新制Cu(OH)2氧化,則乙醛也能被溴水氧化 | |
| D. | HBr的沸點小于HI的沸點,則HBr的穩定性小于HI的穩定性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷與氯氣在光照的條件下制取純凈的一氯甲烷 | |
| B. | 常見的塑料有:①聚乙烯 ②聚丙烯 ③聚氯乙烯 ④聚苯乙烯,其分子內部都含有雙鍵 | |
| C. | 牡丹籽油是一種優良的植物油脂,它可使酸性高錳酸鉀溶液褪色 | |
| D. | 等質量的乙烯和聚乙烯充分燃燒所需氧氣的量不相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2為0.3 mol•L-1、O2為0.2 mol•L-1 | |
| B. | SO3SO2各為0.15 mol•L-1 | |
| C. | O2為0.05 mol•L-1 | |
| D. | SO3為0.3 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 要檢驗某溴乙烷中的溴元素,可以加入NaOH溶液共熱,冷卻后滴入AgNO3溶液,觀察有無淺黃色沉淀生成 | |
| B. | 實驗室制取乙烯時,常伴有刺激性氣味的氣體產生,說明部分乙醇被氧化為乙醛 | |
| C. | 凡是能發生銀鏡反應的物質一定是醛或羧酸中的甲酸 | |
| D. | 向苯酚鈉溶液中通入過量的二氧化碳氣體時,生成物不可能是碳酸鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 作半導體材料的元素大多數位于周期表中金屬元素和非金屬元素的交界處 | |
| B. | 農藥中常含有的元素通常在元素周期表的右上方區域內 | |
| C. | 構成催化劑的元素通常在元素周期表的左下方區域內 | |
| D. | 在周期表過渡元素中尋找作耐高溫和耐腐蝕的合金材料的元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
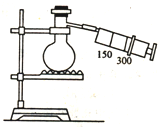 如圖所示(圖中部分儀器未畫出)有一容積為300mL的注射器,與蒸餾燒瓶(500mL)相連接,燒瓶中有0.384g Cu片,現向燒瓶中加入18mL 2.5mol•L-1的稀HNO3溶液,并立即用錫箔包住橡皮塞封住瓶口.(氣體體積視為標準狀況下的)試回答:
如圖所示(圖中部分儀器未畫出)有一容積為300mL的注射器,與蒸餾燒瓶(500mL)相連接,燒瓶中有0.384g Cu片,現向燒瓶中加入18mL 2.5mol•L-1的稀HNO3溶液,并立即用錫箔包住橡皮塞封住瓶口.(氣體體積視為標準狀況下的)試回答:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com