
| A. | 單質的顏色逐漸加深 | B. | 氣態氫化物的穩定性逐漸增強 | ||
| C. | 單質的熔點逐漸升高 | D. | 單質的氧化性逐漸增強 |
分析 A.鹵族元素單質的顏色隨著原子序數增大而依次是淺黃綠色-黃綠色-紅棕色-紫紅色;
B.元素的非金屬性越強,其氫化物的穩定性越強;
C.分子晶體熔沸點與相對分子質量成正比;
D.鹵族元素非金屬性越強,其單質的氧化性越強.
解答 解:A.鹵族元素由上到下,單質的顏色是逐漸加深的,依次是淺黃綠色-黃綠色-紅棕色-紫紅色,故A正確;
B.鹵族元素非金屬性隨著核電荷數增大而減弱,則其氫化物的穩定性隨著原子核電荷數增大而減弱,故B錯誤;
C.鹵族元素單質都是分子晶體,分子晶體熔沸點與相對分子質量成正比,所以隨著核電荷數增大其單質的熔沸點升高,故C正確;
D.鹵族元素非金屬性隨著核電荷數增大而減弱,其單質的氧化性隨著核電荷數增大而減弱,故D錯誤;
故選AC.
點評 本題考查同一主族元素性質遞變規律,為高頻考點,明確非金屬性強弱判斷方法及非金屬性與氫化物的穩定性、單質的氧化性之間的關系即可解答,注意規律中的反常現象,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
| 序號 | 1 | 2 | 3 | 4 | 5 | 6 |
| 導管及儀器 |  |  |  |  |  |  |
| 每個橡皮塞上都打了兩個孔 | ||||||
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(NH3)=0.15 mol/L•min | B. | v(H2)=0.1 mol/L•min | ||
| C. | v(N2)=0.1 mol/L•min | D. | v(N2)=0.002 mol/L•s |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 置換反應的通式可表示為如圖所示:請回答下列問題:
置換反應的通式可表示為如圖所示:請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
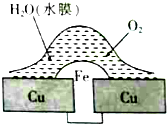
| A. | 此過程中銅被腐蝕 | |
| B. | 此過程中電子從Cu移向Fe | |
| C. | 鐵鉚釘表面發生的電極反應為Fe-3e-═Fe3+ | |
| D. | 在金屬表面刷上一層油漆,能延緩鐵鉚釘的腐蝕 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Zn與稀H2SO4反應:Zn+H+═Zn2++H2↑ | |
| B. | Na2CO3溶液與足量鹽酸反應:CO32-+2H+═H2O+CO2↑ | |
| C. | Cl2與NaOH溶液反應:Cl2+2OH-═2Cl-+H2O | |
| D. | MgCl2溶液與過量氨水反應:Mg2++2OH-═Mg(OH)2↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗現象 | 結論 |
| A | 把相同大小的一塊鋁和鎂分別投入相同濃度的NaOH溶液中:鋁溶解有氣泡放出,而鎂沒有任何變化 | 由此得出:鋁的金屬性比鎂強 |
| B | 取一塊鋁箔,用酒精燈點燃:鋁箔只熔化成液體而沒有脫落 | 由此得出:鋁不易燃燒 |
| C | 向氯化銨溶液中投入一鋁片:鋁片上產生大量氣泡 | 由此得出:該氣體是氨氣 |
| D | 向氯化鋁溶液中逐滴滴加NaOH溶液至過量:先產生白色沉淀,后沉淀逐漸溶解,最后沉淀完全消失 | 由此得出:氫氧化鋁能溶于強堿溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 在化學反應中,只有極少數能量比平均能量高得多的反應物分子發生碰撞時才可能發生化學反應,這些分子稱為活化分子,使普通分子變成活化分子所需提供的最低限度的能量叫活化能,其單位通常用kJ/mol表示.請認真觀察如圖,然后回答問題.
在化學反應中,只有極少數能量比平均能量高得多的反應物分子發生碰撞時才可能發生化學反應,這些分子稱為活化分子,使普通分子變成活化分子所需提供的最低限度的能量叫活化能,其單位通常用kJ/mol表示.請認真觀察如圖,然后回答問題.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 58.5 g的氯化鈉固體中含有NA個氯化鈉分子 | |
| B. | 0.1 L 3 mo1•L-1的NH4NO3溶液中含有的NH4+數目為0.3×6.02×1023 | |
| C. | 5.6 g鐵粉與硝酸反應失去的電子數一定為0.3×6.02×1023 | |
| D. | 4.5 g SiO2晶體中含有的硅氧鍵數目為0.3×6.02×1023 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com