
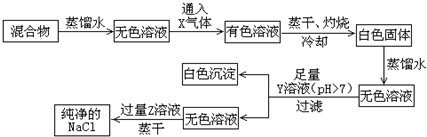
分析 混合物溶于水,通入氣體X可得有色溶液,說明生成溴,則X為Cl2,將溶液蒸干、灼燒得到白色固體含有氯化鈉、氯化鈣,加入蒸餾水溶解,然后加入足量的Y溶液,生成白色 沉淀,Y溶液的pH>7,應為Na2CO3,可與氯化鈣反應生成CaCO3沉淀,濾液中加入過量鹽酸,蒸干可得氯化鈉,以此解答該題.
解答 解:混合物溶于水,通入氣體X可得有色溶液,說明生成溴,則X為Cl2,將溶液蒸干、灼燒得到白色固體含有氯化鈉、氯化鈣,加入蒸餾水溶解,然后加入足量的Y溶液,生成白色 沉淀,Y溶液的pH>7,應為Na2CO3,可與氯化鈣反應生成CaCO3沉淀,濾液中加入過量鹽酸,蒸干可得氯化鈉,
(1)由以上分析可知X為Cl2,Y為Na2CO3,Z為鹽酸,故答案為:Cl2;Na2CO3;鹽酸;
(2)過濾時,除漏斗外還需要的玻璃儀器有燒杯、玻璃棒,故答案為:燒杯、玻璃棒;
(3)混合物中含有氯化鈣,加入碳酸鈉,可使氯化鈣生成沉淀,若在不使用pH試紙的情況下,檢驗Y溶液是否足量的方法是過濾前先靜置,取上層澄清溶液,滴加少量Na2CO3溶液,無沉淀產生(或滴加少量鹽酸有氣泡產生),說明Y溶液是足量的,
故答案為:使溶液中的Ca2+形成CaCO3沉淀;過濾前先靜置,取上層澄清溶液,滴加少量Na2CO3溶液,無沉淀產生(或滴加少量鹽酸有氣泡產生),說明Y溶液是足量的.
點評 本題考查物質的分離、提純,為高頻考點,側重于學生的分析、實驗能力的考查,注意把握物質的性質以及實驗的原理和基本實驗操作方法,難度不大.


 暑假作業海燕出版社系列答案
暑假作業海燕出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | CH3CH3+Cl2$\stackrel{光}{→}$CH3CH2Cl+HCl | |
| B. | 2CH3CH2OH+O2$→_{△}^{催化劑}$2CH3CHO+2H2O | |
| C. | 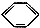 +Br2$\stackrel{Fe}{→}$ +Br2$\stackrel{Fe}{→}$ Br+HBr Br+HBr | |
| D. | CH2═CH2+Br2→CH2Br-CH2Br |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{100W}{36a}$×100% | B. | $\frac{W}{36a+W}$×100% | C. | $\frac{W}{3600a+W}$×100% | D. | $\frac{100W}{36a+W}$×100% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
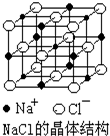 NaCl晶體結構如圖所示,現測知NaCl晶體中Na+與Cl-平均距離為a cm,該晶體密度為ρg•cm-3,則阿伏加德羅常數可表示為( )
NaCl晶體結構如圖所示,現測知NaCl晶體中Na+與Cl-平均距離為a cm,該晶體密度為ρg•cm-3,則阿伏加德羅常數可表示為( )| A. | $\frac{0.585}{4{a}^{3}ρ}$ | B. | $\frac{5.85}{8{a}^{3}ρ}$ | C. | $\frac{58.5}{2{a}^{3}ρ}$ | D. | $\frac{58.5}{{a}^{3}ρ}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/K | 反應I | 反應II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 | |
| 398 | K1′ | K2′ |

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
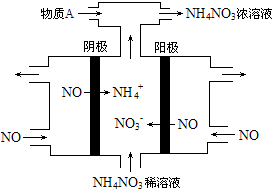 =$\frac{ax}{2}$mol,n(Cl2)=(1-x)a.
=$\frac{ax}{2}$mol,n(Cl2)=(1-x)a.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X是SO2,它既有氧化性又有還原性 | |
| B. | 干燥的氣體Y不能使干燥的有色布條褪色,其水溶液具有漂泊作用的是HClO | |
| C. | Z與水反應的化學方程式為:3NO2+H2O=2HNO3+NO | |
| D. | 等物質的量的X與Y同時通入到濕潤的有色布條上,有色布條褪色時間變短,漂泊效果增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖1是盛硫酸的試劑瓶上的標簽的部分內容,現實驗需要0.5mol•L-1H2SO4溶液480mL,若由你來配制所需溶液,請根據實驗室已有的儀器和藥品情況回答下列問題:
如圖1是盛硫酸的試劑瓶上的標簽的部分內容,現實驗需要0.5mol•L-1H2SO4溶液480mL,若由你來配制所需溶液,請根據實驗室已有的儀器和藥品情況回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com