
| A. | 標準狀況下生成N的體積為$\frac{22.4(n-m)}{51}$L | |
| B. | 沉淀中OH-的質量為17bVg | |
| C. | 恰好溶解后溶液中的NO3-的物質的量為$\frac{bV}{1000}$mol | |
| D. | 與合金反應的硝酸的物質的量為($\frac{n-m}{51}$+$\frac{bV}{1000}$)mol |
分析 mg鋁鎂合金與一定濃度的稀硝酸恰好完全溶解(假定硝酸的還原產物只有NO),向反應后的混合溶液中滴加b mol/L NaOH溶液,當滴加到V mL時,得到沉淀質量恰好為最大值n克,沉淀質量最大為氫氧化鋁和氫氧化鎂質量之和,此時溶液為硝酸鈉溶液,
A、根據電子守恒原理計算生成NO的物質的量,再根據V=nVm計算NO的體積;
B、沉淀為氫氧化鋁和氫氧化鎂,沉淀質量等于鋁鎂合金質量與氫氧根質量之和;
C、恰好溶解后溶液中的NO3-離子的物質的量等于沉淀質量最大溶液中NO3-離子的物質的量,即n(NO3-)=n(Na+)=n(NaOH),據此進行計算;
D、根據質量守恒,硝酸有兩種作用,作為酸的硝酸(生成硝酸鹽)的物質的量等于硝酸鈉的物質的量,作氧化劑的硝酸的物質的量等于NO的物質的量進行計算.
解答 解:A、根據電子守恒原理,生成NO時,HNO3中+5價的N原子得3個電子,因此生成NO的物質的量應該是轉移電子的三分之一,即$\frac{n-m}{17}$mol×$\frac{1}{3}$=$\frac{n-m}{51}$mol,其體積在標準狀況下為$\frac{22.4(n-m)}{51}$L,故A正確;
B、沉淀為氫氧化鋁和氫氧化鎂,沉淀質量等于鋁鎂合金質量與氫氧根質量之和,所以沉淀中氫氧根的質量為(n-m)克,故B錯誤;
C、恰好溶解后溶液中的NO3-離子的物質的量等于沉淀質量最大溶液中NO3-離子的物質的量,當沉淀量最大時,溶液中的溶質只有硝酸鈉(NaNO3),硝酸根離子與鈉離子的物質的量相等,n(NO3-)=n(Na+)=n(NaOH)=$\frac{bV}{1000}$mol,故C正確;
D、參加反應的硝酸有兩種作用,起酸和氧化劑作用,作為酸的硝酸(生成硝酸鹽)的物質的量等于硝酸鈉的物質的量為$\frac{bV}{1000}$mol,作氧化劑的硝酸的物質的量等于NO的物質的量為$\frac{n-m}{51}$mol,所以與合金反應的硝酸的物質的量為($\frac{n-m}{51}$+$\frac{bV}{1000}$)mol,故D正確.
故選:B.
點評 本題結合鋁鎂與硝酸反應及生成的鹽與氫氧化鈉反應的特點,對電子守恒、溶液電中性原理、質量守恒進行綜合考查,難度中等,題目以多項形式呈現,考查了學生的綜合運用知識能力和解決復雜問題的能力,是一道考查能力的好題.


 53天天練系列答案
53天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 3種 | B. | 4種 | C. | 5種 | D. | 6種 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 研究人員發現了一種“水’’電池,其總反應為:5Mn02+2Ag+2NaCl=Na2Mn5O10+2AgCl.如圖用“水”電池為電源電解NaCl溶液的實驗中,X電極上有無色氣體逸出.下列有關分析正確的是( )
研究人員發現了一種“水’’電池,其總反應為:5Mn02+2Ag+2NaCl=Na2Mn5O10+2AgCl.如圖用“水”電池為電源電解NaCl溶液的實驗中,X電極上有無色氣體逸出.下列有關分析正確的是( )| A. | I為負極,其電極反應式為Ag+Cl--e-=AgCl | |
| B. | “水”電池內Na+不斷向負極作定向移動 | |
| C. | 每轉移1mole-,U型管中消耗0.5mol H2O | |
| D. | 開始時U型管中Y極附近pH逐漸增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
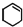 )為原料合成,路線如下(部分反應條件省略):
)為原料合成,路線如下(部分反應條件省略):
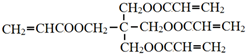
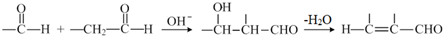

 的化學方程式是
的化學方程式是 .
.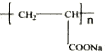
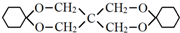 .
. .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 福爾馬林可作食品的保鮮劑 | |
| B. | 聚乙烯塑料制品可作食品的包裝材料 | |
| C. | 碳酸氫鈉可于治療胃酸過多癥 | |
| D. | 食鹽可作調味劑,也可作食品防腐劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 綠色化學的核心就是治理工業生產對環境產生的污染 | |
| B. | 鐵、鈣、碘都是人體必不可少的微量元素 | |
| C. | 食鹽可作調味劑,但不可作食品防腐劑 | |
| D. | “地溝油”經過加工處理后,可以用來制肥皂和生物柴油 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com