

| A. | 該試劑的物質的量濃度為9.2 mol•L-1 | |
| B. | 該硫酸50 mL與足量的銅反應可得到標準狀況下SO2 10.3 L | |
| C. | 硫酸是強電解質 | |
| D. | 該硫酸與等體積的水混合所得溶液的質量分數小于49% |
分析 A、根據c=$\frac{1000ρω}{M}$計算該硫酸溶液的物質的量濃度;
B.根據Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O及Cu與稀硫酸不反應來分析;
C、硫酸是強電解質;
D、根據密度和體積計算溶液的總質量,根據硫酸的密度大于水的密度,判斷質量分數關系;
解答 解:A、該硫酸溶液的物質的量濃度為$\frac{1000×1.84×98%}{98}$mol/L=18.4mol/L,故A錯誤;
B、發生反應:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,隨反應的進行,濃硫酸變為稀硫酸,Cu與稀硫酸不反應,故生成二氧化硫的物質的量小于0.05L×18.4mol/L×0.5×22.4L/mol=10.4L,故B錯誤;
C、硫酸是強酸是強電解質,故C正確;
D、等體積混合,設體積分別為Vml,98%的H2SO4溶液密度為ρ1,水密度為ρ2,則混合后溶液的質量分數為w(H2SO4)=$\frac{V•ρ1×98%}{V•ρ1+V•ρ2}$×100%=$\frac{ρ1×98%}{ρ1+ρ2}$×100%,因硫酸的密度大于水的密度,則ρ1>ρ2,所以=$\frac{ρ1×98%}{ρ1+ρ2}$×100%>49%,故D錯誤;
故選C.
點評 本題考查溶液濃度有關計算,題目難度中等,注意硫酸的濃度越大密度越大,B選項為易錯點,注意濃度的影響.


 優生樂園系列答案
優生樂園系列答案 新編小學單元自測題系列答案
新編小學單元自測題系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
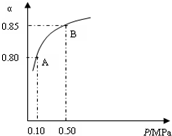
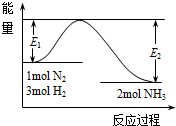 氨是氮循環過程中的重要物質,氨的合成是目前普遍使用的人工固氮方法.
氨是氮循環過程中的重要物質,氨的合成是目前普遍使用的人工固氮方法.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 二氧化硫和氮的氧化物是常用的工業原料,但也是大氣的主要污染物.綜合治理其污染是環境化學當前的重要研究內容之一.
二氧化硫和氮的氧化物是常用的工業原料,但也是大氣的主要污染物.綜合治理其污染是環境化學當前的重要研究內容之一.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增加C,B的平衡轉化率不變 | |
| B. | 此時,B的平衡轉化率是35% | |
| C. | 增大該體系的壓強,平衡向右移動,化學平衡常數增大 | |
| D. | 該反應的化學平衡常數表達式是K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 2:7或5:4 | B. | 2:1或5:4 | C. | 4:5或7:2 | D. | 2:1或7:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 洗滌油污常用熱的碳酸鈉溶液 | |
| B. | 無法利用Na2S溶液和AlCl3溶液制備Al2S3 | |
| C. | 金屬焊接中,可用NH4Cl溶液作除銹劑 | |
| D. | 工業上用FeCl3溶液腐蝕銅制印刷電路板 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com