
關于下圖所示裝置(鹽橋含KCl)的敘述,正確的是
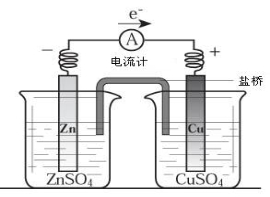
A.銅離子在銅片表面被氧化
B.銅作陽極,銅片上有氣泡產生
C.電流從鋅片經導線流向銅片
D.右側燒杯中,SO42-的物質的量幾乎不變,K+的數目增多
科目:高中化學 來源:2015-2016學年河北正定中學高二上學期第一次聯考化學試卷(解析版) 題型:選擇題
已知HF、CH3COOH均為弱酸,酸性強弱順序為HF>CH3COOH。下列說法不正確的是
A.濃度均為0.1mol·L-1的NaF、CH3COONa溶液相比較,CH3COONa溶液堿性較強
B.0.1mol·L-1CH3COOH溶液,加水稀釋過程中,所有離子濃度均減小
C.NaF溶液中含有Na+、F-、H+、OH-、H2O、HF六種微粒
D.NaF溶液中加入少量NaOH固體,溶液中c(F-)增大
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省高三第一次月考化學試卷(解析版) 題型:填空題
(14分)高錳酸鉀(KMnO4)和過氧化氫(H2O2)是兩種典型的氧化劑。
Ⅰ、(1)H2O2的結構式為______________。
(2)下列物質中能使酸性KMnO4溶液褪色的是________(填選項字母)。
A.臭堿(Na2S) B.小蘇打(NaHCO3)
C.水玻璃(Na2SiO3) D.酒精(C2H5OH)
(3)高錳酸鉀、雙氧水、活性炭常用于飲用水的處理,但三者聯合作用時必須有先后順序。
在稀硫酸中,KMnO4和H2O2能發生氧化還原反應:
氧化反應:H2O2-2e-→2H++O2↑
還原反應:MnO4-+5e-+8H+→Mn2++4H2O
寫出該氧化還原反應的離子方程式________________
Ⅱ、在處理飲用水時,活性炭應在高錳酸鉀反應結束后投加。
(1)請將下列五種物質:KBr、Br2、I2、KI、K2SO4分別填入下列橫線上,組成一個未配平的化學方程式:
KBrO3+________+H2SO4―→________+________+________+________+H2O。
(2)如果該化學方程式中I2和KBr的化學計量數分別是8和1,則:
①Br2的化學計量數是________;
②請將反應物的化學式及配平后的化學計量數填入下列相應的位置中:

③若轉移10 mol e-,則反應后生成I2的物質的量為________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西陽泉十五中高三第一次階段考試化學試卷(解析版) 題型:選擇題
下列有關說法中,正確的是
A.鹽酸、漂白粉都是混合物 B.127I和131I互為同素異形體
C.硫酸銅、二氧化硫都是電解質 D.分餾、干餾都是物理變化
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河南省三門峽市高二上學期入學考試化學試卷(解析版) 題型:選擇題
反應2Z(g)===X(g)+ Y(g) ,△H>0.達到平衡時,下列說法正確的是
A.加入催化劑,X的產率增大
B.升高溫度,Y的轉化率增大
C.當容器活塞可活動時,充入稀有氣體,平衡不移動
D.充入Z氣體時,Z的轉化率增大
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二上學期第一次月考化學試卷(解析版) 題型:填空題
(14分)(1)今有2H2+O2 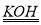 2H2O反應,構成燃料電池,則負極通入的應是 ,正極通的應是 。電極反應式為正極: ;負極: ;
2H2O反應,構成燃料電池,則負極通入的應是 ,正極通的應是 。電極反應式為正極: ;負極: ;
(2)若把KOH溶液改為稀H2SO4作電解質,則電極反應式為
正極: ;負極: ;
(1)和(2)的電解質不同,反應后,其溶液的pH各有什么變化? ;
(3)若把H2改為CH4,用KOH溶液作電解質溶液,則負極的電極反應式為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二上學期第一次月考化學試卷(解析版) 題型:選擇題
綠色能源是指使用過程中不排放或排放極少污染物的能源,如一級能源中的水能、地熱、天然氣等;二級能源中電能、氫能等。下列能源屬于綠色能源的是
①太陽能 ②風能 ③石油 ④煤 ⑤潮汐能 ⑥木材
A.①②③ B.③④⑤ C.④⑤⑥ D.①②⑤
查看答案和解析>>
科目:高中化學 來源:2015-2016學年貴州省高二上第一半月考化學試卷(解析版) 題型:選擇題
已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-568 kJ·mol-1
②H2(g)+1/2O2(g)===H2O(g) ΔH=-248 kJ·mol-1
已知CO和H2的混合物1 mol在氧氣中充分燃燒放出的熱量272 kJ,則該混合氣體中CO和氫氣的物質的量的比值為
A.1∶1 B.3∶37
C.2∶1 D.3∶2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高一入學摸底化學試卷(解析版) 題型:計算題
一定量的氫氣在氯氣中燃燒,所得混合物用100mL6.00mol/L的NaOH溶液(密度為1.2g/mL)恰好完全吸收,測得溶液中含有NaClO的物質的量為0.1000mol.
(1)原NaOH溶液的質量分數為 .
(2)所得溶液中Cl﹣的物質的量為 mol.
(3)所用氯氣和參加反應的氫氣的物質的量之比n(Cl2):n(H2)= .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com