
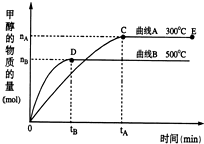
 一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)
一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |


 新卷王期末沖刺100分系列答案
新卷王期末沖刺100分系列答案 全能闖關100分系列答案
全能闖關100分系列答案科目:高中化學 來源: 題型:
| A、鈉在空氣中燃燒后發出黃色的火焰 |
| B、Na2O2是淡黃色固體,是強氧化劑,可用來漂白織物等 |
| C、氧化劑在化學反應中得到電子,所含元素化合價都降低 |
| D、離子方程式的書寫時弱電解質、單質等寫成化學式 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、a%>b% | B、a%<b% |
| C、a%=b% | D、無法判定 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、構成原電池的正極和負極的材料必須是兩種活潑性不同的金屬 |
| B、原電池是把化學能轉變為電能的裝置 |
| C、把銅片插入FeCl3溶液中,在銅片表面出現一層鐵 |
| D、原電池工作時,正極和負極上發生的都是氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
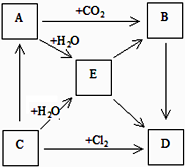 如圖表示A、B、C、D、E五種物質的相互轉化關系,其中A為淡黃色固體,C為金屬單質,D為最常用的調味品.
如圖表示A、B、C、D、E五種物質的相互轉化關系,其中A為淡黃色固體,C為金屬單質,D為最常用的調味品.查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
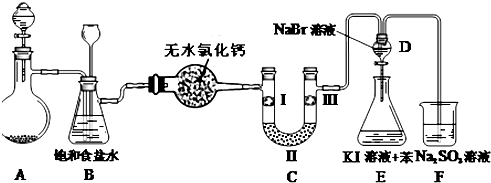
| a | b | c | |
| I | 干燥的有色布條 | 濕潤的有色布條 | 濕潤的有色布條 |
| II | 堿石灰 | 濃硫酸 | 無水氯化鈣 |
| III | 濕潤的有色布條 | 干燥的有色布條 | 干燥的有色布條 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 族周期 | ⅠA | ⅡA | Ⅲ | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | e | ||||
| 3 | f | g | h | i | j | k | m | n |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com