
| 族周期 | ⅠA | ⅡA | Ⅲ | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | a | |||||||
| 2 | b | c | d | e | ||||
| 3 | f | g | h | i | j | k | m | n |


 舉一反三單元同步過關卷系列答案
舉一反三單元同步過關卷系列答案科目:高中化學 來源: 題型:
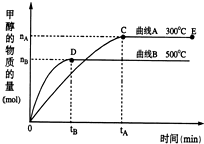 一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)
一定條件下,在體積為3L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g)?CH3OH(g)| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
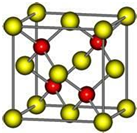 有A、D、E、G、M、L六種前四周期的元素.A是宇宙中最豐富的元素.D原子核外有1個未成對電子,D+比E原子少一個電子層,E原子得一個電子填入3p軌道后,3p軌道呈全充滿狀態.G原子的2p軌道有2個未成對電子,M的最高化合價和最低化合價的代數和為4,與G的原子序數相差8.L位于周期表第12縱行且是六種元素中原子序數最大的.R是由M、L形成的化合物,其晶胞結構如圖所示.請回答下列問題:
有A、D、E、G、M、L六種前四周期的元素.A是宇宙中最豐富的元素.D原子核外有1個未成對電子,D+比E原子少一個電子層,E原子得一個電子填入3p軌道后,3p軌道呈全充滿狀態.G原子的2p軌道有2個未成對電子,M的最高化合價和最低化合價的代數和為4,與G的原子序數相差8.L位于周期表第12縱行且是六種元素中原子序數最大的.R是由M、L形成的化合物,其晶胞結構如圖所示.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| 高溫 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com