
分析 (1)依據熱化學方程式和蓋斯定律計算得到所需熱化學方程式,①-②×3得到Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)和反應焓變;
(2)①依據化學方程式和平衡常數概念寫出平衡常數表達式,平衡常數=$\frac{生成物平衡濃度系數次冪之積}{反應物平衡濃度系數次冪之積}$;
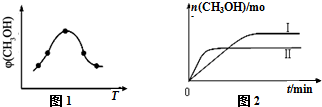
②由圖可知最高點反應到達平衡,到達平衡后,溫度越高,φ(CH3OH)越小,升高溫度平衡向逆反應進行,據此判斷;
③由圖象分析先拐先平,溫度高TⅡ先達到平衡則TⅡ>TⅠ,縱軸是甲醇的物質的量,溫度越高,甲醇越少,平衡逆向進行分析判斷;
(3)①根據反應物、反應條件、生成物寫出,反應物是二氧化碳和氨氣(NH3),反應條件是高溫、高壓,生成物是尿素[CO(NH2)2]和水;
②根據原電池原理,CO2在正極發生還原反應轉化為甲烷,注意電解質溶液為酸性.
解答 解:(1)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
依據蓋斯定律①-②×3得到Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1;
故答案為:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1;
(2)①平衡常數等于生成物的濃度冪之積除以反應物的濃度冪之積,所以K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$,
故答案為:$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$;
②由圖可知最高點反應到達平衡,達平衡后,溫度越高,φ(CH3OH)越小,平衡向逆反應進行,升高溫度平衡吸熱方向進行,逆反應為吸熱反應,則正反應為放熱反應,即△H<0,
故答案為:<;
③由圖2可知,溫度TⅠ<TⅡ,平衡時,溫度越高CO的轉化率越小,說明升高溫度,平衡向逆反應移動,升高溫度平衡向吸熱反應移動,故該反應正反應為放熱反應,則△H<0,升高溫度,平衡向逆反應移動,所以KⅠ>KⅡ,
故答案為:>;
(3)①根據反應物是二氧化碳和氨氣(NH3),反應條件是高溫、高壓,生成物是尿素[CO(NH2)2]和水,化學反應式為2NH3+CO2$\frac{\underline{\;一定條件\;}}{\;}$CO(NH2)2+H2O,
故答案為:2NH3+CO2$\frac{\underline{\;一定條件\;}}{\;}$CO(NH2)2+H2O;
②CO2在正極發生還原反應轉化為甲烷,考慮電解質為硫酸,所以甲烷中氫來源為硫酸電離的氫離子,根據化合價變化可知1mol二氧化碳變成甲烷得到8mol電子,故電極反應為:CO2+8e-+8H+=CH4+2H2O,
故答案為:CO2+8e-+8H+=CH4+2H2O.
點評 本題考查了熱化學方程式的書寫、化學平衡移動、平衡常數概念理解、轉化率的計算及原電池原理的分析應用等,題目涉及的知識點較多,綜合性較強,難度中等.分析圖象時,要考慮先拐先平衡的原則,則反應條件為溫度高或壓強大,寫電極反應式一定要考慮介質的參與.


 A加金題 系列答案
A加金題 系列答案 全優測試卷系列答案
全優測試卷系列答案科目:高中化學 來源: 題型:解答題
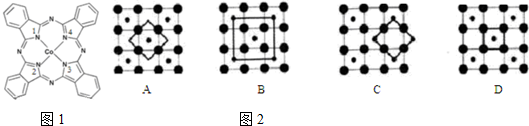
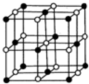 ),在該晶體中與一個鈷原子等距離且最近的鈷原子有12個;筑波材料科學國家實驗室一個科研小組發現了在 5K 下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如2所示,小球表示Co原子,大球表示O原子).下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成的是D.
),在該晶體中與一個鈷原子等距離且最近的鈷原子有12個;筑波材料科學國家實驗室一個科研小組發現了在 5K 下呈現超導性的晶體,該晶體具有CoO2的層狀結構(如2所示,小球表示Co原子,大球表示O原子).下列用粗線畫出的重復結構單元示意圖不能描述CoO2的化學組成的是D.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 離子半徑:N3->F->Na+ | |
| B. | 上述反應除①外都是氧化還原反應 | |
| C. | 反應②③中的水做氧化劑,每生成1mol H2,轉移的電子數為2NA | |
| D. | 反④中的水是還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在酒精燈加熱條件下,Na2CO3、NaHCO3固體都能發生分解 | |
| B. | Fe(OH)3膠體無色、透明,能發生丁達爾現象 | |
| C. | H2、SO2、CO2三種氣體都可用濃硫酸干燥 | |
| D. | Na2O和Na2O2投入水中都能生成NaOH,都是氧化還原反應,它們都是堿性氧化物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 體積之比是2:3 | B. | 原子數之比是3:2 | ||
| C. | 質子數之別是1:1 | D. | 物質的量之比是1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 標準狀況下,22.4L水所含有的原子數目為3NA | |
| B. | 標準狀況下,22.4 L H2中含質子數為2NA | |
| C. | 0.1mol•L-1稀硫酸100mL中含有硫酸根個數為0.1NA | |
| D. | 0.1molOH-含NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗編號 | ① | ② | ③ | ④ |
| 稀硝酸體積/mL | 100 | 200 | 300 | 400 |
| 剩余金屬質量/g | 9.0 | 4.8 | 0 | 0 |
| NO體積/L | 1.12 | 2.24 | 3.36 | V |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | O2 MnO2 KMnO4 | B. | KMnO4 MnO2O2 | ||
| C. | MnO2KMnO4 O2 | D. | O2 KMnO4 MnO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com