
| A. | 離子半徑:N3->F->Na+ | |
| B. | 上述反應除①外都是氧化還原反應 | |
| C. | 反應②③中的水做氧化劑,每生成1mol H2,轉移的電子數為2NA | |
| D. | 反④中的水是還原劑 |
分析 A.電子層越多,半徑越大,電子層一樣,核電荷數越多,半徑越小;
B.有元素化合價變化的反應是氧化還原反應;
C.②NaH+H2O=NaOH+H2↑,H2O中H化合價降低;③2Na+2H2O=2NaOH+H2↑,H2O中H化合價降低;
D.④2F2+2H2O=4HF+O2,H2O中O化合價升高.
解答 解:A.電子層一樣,核電荷數越多,半徑越小,所以N3->F->Na+,故A正確;
B.①Na3N+H2O=NaOH+NH3 該反應中沒有元素化合價發生變化,不屬于氧化還原反應,其余都有化合價變化,屬于氧化還原反應,故B正確;
C.②NaH+H2O=NaOH+H2↑,H2O中H化合價降低為氧化劑,轉移電子數為1e-,則每生成1mol H2,轉移的電子數為1NA,③2Na+2H2O=2NaOH+H2↑,H2O中H化合價降低為氧化劑,轉移電子數為2e-,則每生成1mol H2,轉移的電子數為2NA,故C錯誤;
D.④2F2+2H2O=4HF+O2,H2O中O化合價升高,所以水是還原劑,故D正確;
故選:C.
點評 本題考查了鈉及其化合物的性質,涉及離子半徑大小比較、氧化還原反應的判斷以及電子轉移的計算等,題目難度不大,把握氧化還原反應的規律,準確判斷元素的化合價是解題關鍵.


 快捷英語周周練系列答案
快捷英語周周練系列答案科目:高中化學 來源: 題型:解答題
| 滴定次數 | 待測溶液的體積/mL | 標準溶液的體積 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.05 |
| 2 | 25.00 | 2.00 | 22.01 |
| 3 | 25.00 | 0.50 | 21.50 |
| 4 | 25.00 | 0.20 | 20.22 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
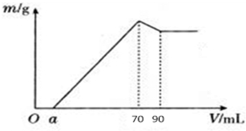
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A+3B═C | B. | 2A+B═C | C. | A+3B═2C | D. | A+3B═3C |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 根據氧化物的性質可將氧化物分成酸性氧化物、堿性氧化物、兩性氧化物和特殊氧化物等 | |
| B. | 根據反應中是否有電子轉移將化學反應分為氧化還原反應和非氧化還原反應 | |
| C. | 根據分散質粒子直徑大小可將液體分散系分為溶液、膠體和濁液 | |
| D. | 根據電解質的水溶液導電能力的強弱將電解質分為強電解質和弱電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | MnO2與濃鹽酸反應制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| B. | 碳酸鈣與醋酸溶液反應:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 200mL2mol/L的FeBr2溶液中通入11.2L標準狀況下的氯氣:4Fe2++6Br-+5Cl2═4Fe3++3Br2+10Cl- | |
| D. | Na2S的水解:S2-+2H2O?H2S+2OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
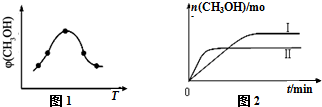
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com