
 鐵是日常生活中用途最廣、用量最大的金屬材料.
鐵是日常生活中用途最廣、用量最大的金屬材料.分析 (1)連接好裝置后,把導管末端插入水中,微熱試管,根據壓強和導管中水柱的變化判斷;
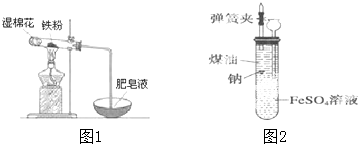
(2)①濕棉花含有水蒸氣,對反應來說提供了水,鐵在高溫下與水反應生成四氧化三鐵和氫氣,據此分析解答即可;
②產物四氧化三鐵中有+2價的鐵和+3價的鐵,還有可能有過量的鐵;
(3)①鈉的密度大于煤油的密度且和煤油不反應,鈉與水反應生成氫氣;
②鈉與硫酸亞鐵溶液反應,是鈉與水反應生成氫氧化鈉,氫氧化鈉與硫酸亞鐵反應生成氫氧化亞鐵沉淀.
解答 解:(1)連接好裝置后,把導管末端插入水中,微熱試管,裝置內的氣體受熱膨脹,在導管末端會產生氣泡,停止加熱,導管內會形成一段水柱,而且水柱保持不變,說明裝置氣密性良好,
故答案為:把導管末端插入水中,微熱試管,在導管末端會產生氣泡,停止加熱,導管內會形成一段水柱,而且水柱保持不變,說明裝置氣密性良好;
(2)①因為是鐵和水蒸氣的反應,試管內有鐵粉,所以濕棉花主要是提供水蒸氣;鐵在高溫下與水反應生成四氧化三鐵和氫氣,反應方程式為3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,
故答案為:提供水蒸氣;3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
②鐵和水蒸氣反應,產物為四氧化三鐵和氫氣,加入過量鹽酸,固體完全溶解,必發生反應:Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,所以所得溶液中存在的陽離子是一定有Fe2+、H+,四氧化三鐵黑色固體中可能含有過量的鐵,可能將三價鐵離子全部轉化成二價鐵離子,Fe+2Fe3+═3Fe2+,所以所得溶液中存在的陽離子是一定有Fe2+、H+,可能有Fe3+,
故答案為:b;
(3)①鈉的密度大于煤油的密度且和煤油不反應,所以鈉在煤油中逐漸下沉;鈉的密度小于水的密度,所以在水中會浮在水面上,鈉的熔點較低,所以鈉在水中會熔成小球;鈉和FeSO4溶液中溶劑反應生成氫氣,所以生成的氫氣推動鈉上浮至煤油層;
故答案為:有氣泡生成,鈉熔化成小球且在煤油和FeSO4溶液界面處上下跳動,最終完全溶解;
②鈉與硫酸亞鐵溶液反應,是鈉與水反應生成氫氧化鈉,氫氧化鈉與硫酸亞鐵反應,所以反應的離子方程式為2Na+Fe2++2H2O═Fe(OH)2↓+2Na++H2↑,
故答案為:2Na+Fe2++2H2O═Fe(OH)2↓+2Na++H2↑.
點評 本題考查Fe、Na的化學性質、性質實驗方案的設計,把握物質的性質、發生的反應等為解答的關鍵,側重分析與實驗能力的考查,注意氧化還原反應的應用,題目難度中等.


 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1個 | B. | 0個 | C. | 2個 | D. | 4個 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaCl、HCl、H2O、NaOH | B. | Cl2、Na2S、HCl、SO2 | ||
| C. | Na2O2、H2O2、H2O、O3 | D. | HBr、CO2、H2O、CS2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
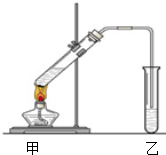 (1)配置混合溶液時,加入試劑的正確順序是A(填“A”或“B”);
(1)配置混合溶液時,加入試劑的正確順序是A(填“A”或“B”);查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 應用下列裝置,在硬質玻璃管中放入還原鐵粉和石棉絨的混合物加熱,并通入水蒸氣,就可以完成“高溫下,Fe與水蒸氣的反應實驗”.
應用下列裝置,在硬質玻璃管中放入還原鐵粉和石棉絨的混合物加熱,并通入水蒸氣,就可以完成“高溫下,Fe與水蒸氣的反應實驗”.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 己二酸
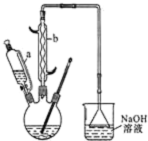
己二酸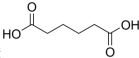 是一種工業上具有重要意義的有機二元酸,在化工生產、有機合成工業、醫藥、潤滑劑制造等方面都有重要作用,能夠發生成鹽反應、酯化反應等,并能與二元醇縮聚成高分子聚合物等,己二酸產量居所有二元羧酸中的第二位.實驗室合成己二酸的反應原理和實驗裝置示意圖如圖:
是一種工業上具有重要意義的有機二元酸,在化工生產、有機合成工業、醫藥、潤滑劑制造等方面都有重要作用,能夠發生成鹽反應、酯化反應等,并能與二元醇縮聚成高分子聚合物等,己二酸產量居所有二元羧酸中的第二位.實驗室合成己二酸的反應原理和實驗裝置示意圖如圖:
| 物質 | 密度(20℃) | 熔點 | 沸點 | 溶解性 | 相對分子質量 |
| 環己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃時水中溶解度3.6g,可混溶于乙醇、苯 | 100 |
| 己二酸 | 1.36g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃時1.44g,25℃時2.3g,易溶于乙醇,不溶于苯 | 146 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
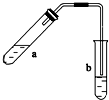 可用圖示裝置制取少量乙酸乙酯(部分圖中均已略去).請填空:
可用圖示裝置制取少量乙酸乙酯(部分圖中均已略去).請填空:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com