
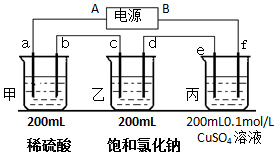
 用上面的電池對下物質進行電解,其中a、b、c、d、e、f電極均為惰性電極,通電后,a極產生的氣體明顯多于b極,2分鐘后,測得乙池的pH為12,則
用上面的電池對下物質進行電解,其中a、b、c、d、e、f電極均為惰性電極,通電后,a極產生的氣體明顯多于b極,2分鐘后,測得乙池的pH為12,則分析 甲池實際上是電解水,生成氫氣和氧氣,氫氣的體積大于氧氣的體積,而a極產生的氣體明顯多于b極,說明a是氫離子放電生成氫氣,b是氫氧根離子放電生成氧氣,乙池是電解飽和食鹽水,生成氫氣、氯氣和氫氧化鈉,而丙是電解硫酸銅生成銅和、氧氣和硫酸,由此分析解答.
解答 解:①說明a是氫離子在陰極放電生成氫氣,所以相連的A極是負極,故答案為:負;
②c極是陰極,是水電離出的氫離子放電,生成氫氣,電極反應式為2H++2e-=H 2↑,故答案為:2H++2e-=H 2↑;
③2分鐘后,測得乙池的pH為12,所以氫氧化鈉的物質的量為:10-2×0.2=2×10-3mol,整個電路轉移電子的數目為2×10-3mol,而乙池中生成氣體的物質的量為2×10-3mol,則甲生成氣體的物質的量之和為:1.5×10-3mol,生成氣體的總物質的為3.5×10-3,故答案為:3.5×10-3;
④生成銅的物質的量為:1×10-3mol,所以質量為:0.064g,生成氫離子的物質的量為:2×10-3mol,所以氫離子的濃度為:$\frac{2×1{0}^{-3}mol}{0.2L}$=0.01mol/L,則溶液的pH為2,故答案為:0.064;2;
⑤電解n分鐘后,硫酸銅正好消耗完,再將e、f電極反接電源,用同樣的電流再電解n分鐘,說明轉移電子的物質的量相等,而體積不變,說明硫酸銅的物質的量濃度為0.1mol/L,故答案為:0.1.
點評 本題為電化學知識的綜合應用,做題時要注意根據電極反應現象判斷出電解池的陰陽級,進而判斷出電源的正負極,要注意三個電解池為串聯電路,各電極上得失電子的數目相等.做題時要正確寫出電極方程式,準確判斷兩極上離子的放電順序.


 課堂全解字詞句段篇章系列答案
課堂全解字詞句段篇章系列答案 步步高口算題卡系列答案
步步高口算題卡系列答案科目:高中化學 來源: 題型:多選題
| A. | 元素的非金屬性次序為c>b>a | |
| B. | a-的還原性弱于c-的還原性 | |
| C. | d和其他3種元素均能形成離子化合物 | |
| D. | 元素a、b、c各自最高和最低化合價的代數和分別為0、4、6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 該裝置的能量轉化方式為太陽能轉化為電能 | |
| B. | 工作時,陽極附近pH減小 | |
| C. | 電路中每轉移4mol電子,捕獲44g二氧化碳 | |
| D. | 陰極的電極反應為CO2+2e-=CO+O2- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 敘述Ⅰ | 敘述Ⅱ |
| A | Fe3+有氧化性 | 用KSCN溶液可以鑒別Fe3+ |
| B | 濃硫酸有腐蝕性 | 常溫下濃硫酸不能用鐵罐盛裝 |
| C | Cl2是非金屬單質 | Cl2能使濕潤的有色布條褪色 |
| D | 熔融狀態的Al2O3中有自由移動的Al3+和O2- | 電解熔融狀態的Al2O3制備Al |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙酸的結構簡式 C2H4O2 | B. | 氯化鈉的電子式: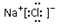 | ||
| C. | 硫原子的原子結構示意圖: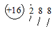 | D. | 水的電離方程式 2H2O═H3O++OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 糖類、油脂、蛋白質都能發生水解反應 | |
| B. | 甲烷和Cl2的反應與乙烯和Br2的反應屬于同一類型的反應 | |
| C. | 苯不能使溴的四氯化碳溶液褪色,但能與H2發生加成反應 | |
| D. | 因分子中均含有官能團“-OH”,故乙醇、乙酸水溶液均呈酸性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | W、M的離子半徑為M<W | |
| B. | YZ2為直線形的共價化合物,W2Z2既含有離子鍵又含有共價鍵 | |
| C. | Z與X形成的化合物的熔沸點偏高是因其分子內存在氫鍵 | |
| D. | Z與M形成的化合物可作為耐高溫材料 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com