


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| A、Na2CO3 |
| B、MgCl2 |
| C、NH4Cl |
| D、NaCl |
查看答案和解析>>
科目:高中化學 來源: 題型:
| | 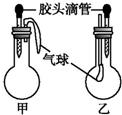 | 甲 | 乙 | |||
| A | 滴管中 | 燒瓶中 | 滴管中 | 燒瓶中 | ||
| B | ||||||
| 水 | 過氧化鈉 | 飽和碳酸氫鈉溶液 | CO2 | |||
| C | ||||||
| 水 | 鈉 | 碳酸鈉溶液 | CO2 | |||
| D | ||||||
| 水 | 氧化鈉 | NaOH溶液 | CO2 | |||
| 稀鹽酸 | 碳酸氫鈉 | NaOH溶液 | CO | |||
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
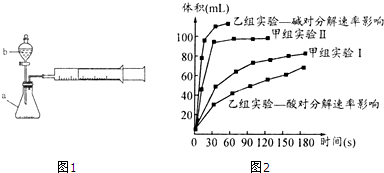
| 實驗編號 | 實驗目的 | t℃ | 催化劑 | 濃度 |
| 甲組實驗Ⅰ | 做實驗參照 | 25 | 3滴FeCl3溶液 | 10ml 2% H2O2 |
| 甲組實驗Ⅱ | 25 | 10ml 5% H2O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
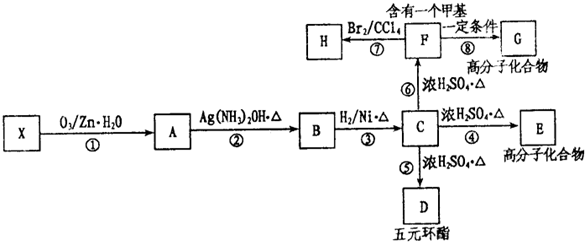
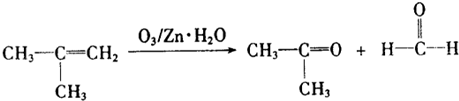
查看答案和解析>>
科目:高中化學 來源: 題型:
 某化學課外活動小組從實驗室取出硫酸試劑,試劑瓶上標簽的部分內容如圖所示.該小組欲配制450mL 0.4mol?L-1的稀硫酸溶液:
某化學課外活動小組從實驗室取出硫酸試劑,試劑瓶上標簽的部分內容如圖所示.該小組欲配制450mL 0.4mol?L-1的稀硫酸溶液:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NH4Cl |
| B、NaOH |
| C、Na2CO3 |
| D、干冰 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com