
| A. | 每生成0.3molH2,被還原的水分子數目為0.6NA | |
| B. | 當有2.7gAl參加反應時,轉移的電子數目為0.3NA | |
| C. | 每生成6.72L的H2,溶液中AlO2-的數目就增加0.2NA | |
| D. | 溶液中每增加0.1mol的AlO2-,Na+的數目就增加0.1NA |
分析 該反應中鋁失電子作還原劑,氫元素得電子作氧化劑,只有水作氧化劑,再根據各種微粒之間的關系式計算,注意弱根離子易水解,據此進行解答.
解答 解:該反應中鋁失電子作還原劑,氫元素得電子作氧化劑,所以只有水作氧化劑,
A.反應過程為:2Al+6H2O═2Al(OH)3+3H2↑,Al(OH)3+2NaOH═NaAlO2+2H2O,由2Al+6H2O═2Al(OH)3+3H2↑可知,每生成0.3 mol H2,被還原的水分子數目為0.6NA,故A正確;
B.根據方程式知,當有2.7 g Al參加反應時,轉移的電子數目=$\frac{2.7g}{27g/mol}$×3×NA=0.3NA,故B正確;
C.沒有指出在標準狀況下,不能使用標準狀況下的氣體摩爾體積計算氫氣的物質的量,故C錯誤;
D.偏鋁酸鈉化學式中Na+和AlO2-的個數之比是1:1,但在溶液中,AlO2-易水解而Na+不水解,導致Na+個數大于AlO2-個數,所以溶液中每增加0.1 mol的AlO2-,Na+的數目增加量大于0.1 NA,故D錯誤;
故選AB.
點評 本題考查了氧化還原反應的計算、物質的量的計算,題目難度不大,明確發生反應的實質為解答關鍵,注意掌握電子守恒的應用方法,試題培養了學生的分析能力及化學計算能力.


科目:高中化學 來源: 題型:解答題
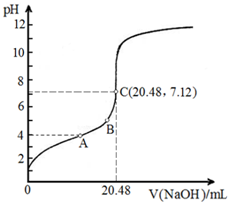 請完成并配平上列的離子方程式.
請完成并配平上列的離子方程式.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯能使酸性高錳酸鉀溶液褪色,發生了加成反應 | |
| B. | 苯可以使溴水褪色,發生了取代反應 | |
| C. | 乙醛在一定條件下與氫氣反應生成乙醇,發生了氧化反應 | |
| D. | 苯在一定條件下能與濃硝酸反應得到硝基苯,發生了取代反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4mol | B. | 1mol | C. | 8mol | D. | 2mol |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
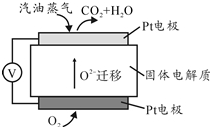 為擺脫對石油的過度依賴,科研人員將煤液化制備汽油,并設計了汽油燃料電池,電池工作原理如圖所示:一個電極通入氧氣,另一電極通入汽油蒸氣,電解質是摻雜了Y2O3的ZrO2晶體,它在高溫下能傳導O${\;}_{2}^{-}$
為擺脫對石油的過度依賴,科研人員將煤液化制備汽油,并設計了汽油燃料電池,電池工作原理如圖所示:一個電極通入氧氣,另一電極通入汽油蒸氣,電解質是摻雜了Y2O3的ZrO2晶體,它在高溫下能傳導O${\;}_{2}^{-}$查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com