

分析 (1)銅和濃硫酸加熱一生成二氧化硫氣體,二氧化硫比空氣重,用向上排氣法收集,進氣的導氣管長進短處;
(2)①銅和濃硫酸加熱反應生成硫酸銅、二氧化硫和水;依據化學方程式中元素化合價變化計算氧化還原關系;
②證明硫酸剩余是證明氫離子的存在;
③濃硫酸隨反應進行濃度變稀后不與銅發生反應;
(3)方案一,堿石灰增重為二氧化硫和水蒸氣的質量分析;
方案二,硫酸鋇沉淀是二氧化硫被氧化為硫酸生成的硫酸鋇沉淀和硫酸酸化高錳酸鉀溶液,氣酸化作用的硫酸生成的硫酸鋇沉淀.
解答 解:(1)銅和濃硫酸加熱一生成二氧化硫氣體,二氧化硫比空氣重,用向上排氣法收集,進氣的導氣管長進短處,圖中補進氣管伸入近集氣瓶底,裝置圖為: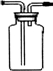 ,故答案為:
,故答案為: ;
;
(2)①銅和濃硫酸加熱反應生成硫酸銅、二氧化硫和水,反應的化學方程式為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;分析化學方程式若有m g銅物質的量為$\frac{m}{64}$mol參加了反應,被還原硫酸物質的量為$\frac{m}{64}$mol,電子轉移物質的量為$\frac{m}{64}$mol×2=$\frac{m}{32}$mol,
故答案為:Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;$\frac{m}{64}$;$\frac{m}{32}$NA;
②能證明反應停止后燒瓶中有硫酸剩余,只能證明氫離子的存在才能說明,不能證明硫酸根離子,因為濃硫酸和銅反應生成了硫酸銅;
A.硫酸鈉溶液不能能證明硫酸根離子存在,也不能證明氫離子的存在,故A不符合;
B.氯化鋇溶液能證明硫酸根離子存在,但不能證明氫離子存在,故B不符合;
C.銀粉和稀硫酸不反應不能證明氫離子的存在,故C不符合;
D.碳酸鈉溶液和氫離子反應生成二氧化碳氣體,可以用來證明溶液中存在稀硫酸,故D符合;
故答案為:D;
③有一定量的硫酸剩余但未能使銅片完全溶解,因為濃硫酸隨反應進行濃度變稀后不與銅發生反應,故答案為:稀硫酸不與銅反應;
(3)方案一:銅和濃硫酸反應生成的二氧化硫氣體中含有水蒸氣,堿石灰吸收的質量為二氧化硫和水蒸氣,或裝置中二氧化硫未被完全排除,稱量的不全是二氧化硫質量,
故答案為:水蒸氣;燒瓶中的二氧化硫不能完全排出;
方案二:生成的沉淀是高錳酸鉀溶液中起酸化作用的硫酸與氯化鋇反應而產生的沉淀和二氧化硫被氧化為硫酸生成的硫酸鋇沉淀,不全是二氧化硫轉化為硫酸生成的沉淀,
故答案為:高錳酸鉀溶液中起酸化作用的硫酸.
點評 本題考查性質實驗方案的設計,題目難度中等,明確實驗目的及實驗原理為解答關鍵,注意隨反應進行濃硫酸變為稀硫酸后不與銅發生反應,試題側重考查學生的分析能力及化學實驗能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
 反應類型:加聚反應
反應類型:加聚反應 +3HNO3$→_{△}^{濃硫酸}$
+3HNO3$→_{△}^{濃硫酸}$ +3H2O.
+3H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 試用分液漏斗分液時,應將漏斗頸上的玻璃塞打開 | |
| B. | 蒸餾實驗不一定使用溫度計 | |
| C. | 用CCl4萃取碘水中的碘 | |
| D. |  過濾(如圖)時,可將懸濁液從燒杯直接倒入漏斗中 過濾(如圖)時,可將懸濁液從燒杯直接倒入漏斗中 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
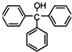 )是一種重要的化工原料和醫藥中間體,實驗室合成三苯甲醇其合成流程如圖1所示,裝置如圖2所示.
)是一種重要的化工原料和醫藥中間體,實驗室合成三苯甲醇其合成流程如圖1所示,裝置如圖2所示. ;
;
| 物質 | 熔點 | 沸點 | 溶解性 |
| 三苯甲醇 | 164.2℃ | 380℃ | 不溶于水,溶于乙醇、乙醚等有機溶劑 |
| 乙醚 | -116.3℃ | 34.6℃ | 微溶于水,溶于乙醇、笨等有機溶劑 |
| 溴苯 | -30.7℃ | 156.2℃ | 不溶于水,溶于乙醇、乙醚等多數有機溶劑 |
| 苯甲酸已酯 | -34.6℃ | 212.6℃ | 不溶于水 |
| Mg(OH)Br | 常溫下為固體 | 能溶于水,不溶于醇、醚等有機溶劑 | |
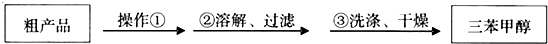
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 1將一小塊金屬鈉放入滴有酚酞溶液的冷水中 2將一小段用砂紙打磨后的鎂帶,放入試管中,加入少量水,加熱至水沸騰,再向試管中滴加酚酞溶液 3將一小段鎂帶投入稀鹽酸中 4將一小片鋁投入稀鹽酸中. |
| 實驗現象 | A劇烈反應,迅速生成大量的氣體 B浮在水面上,熔成小球,不斷游動,小球漸小最終消失,溶液變紅 C反應不劇烈,產生無色氣體 D有氣體產生,溶液變成紅色 |
| 實驗步驟 | 1 | 2 | 3 | 4 |
| 實驗現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
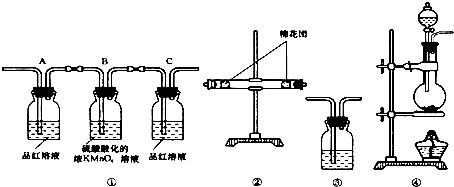
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 生成物是丙酮 | |
| B. | 1-丙醇發生了還原反應 | |
| C. | 反應中有紅黑顏色交替變化的現象發生 | |
| D. | 醇類都能發生圖示的催化氧化反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com