
| A. | 四種物質中一定有共價化合物 | B. | 四種物質中一定有Ba(OH)2 | ||
| C. | 丙溶液加熱蒸干可得原無水溶質 | D. | 丁溶液中含有HCO3- |
分析 由②0.1mol•L-1乙溶液中c(H+)>0.1mol•L-1可知乙溶液為多元酸,再根據所給八種離子可知乙溶液為:H2SO4;
由①甲溶液分別與其它三種溶液混合,均產生白色沉淀,再結合乙溶液為硫酸,可知甲溶液中含有Ba2+,再結合溶液中其他離子可知甲溶液為Ba(OH)2;
由③向丙溶液中滴入AgNO3溶液,產生不溶于稀HNO3的白色沉淀,可知丙溶液中有Cl-,丙溶液中的陽離子不能確定;
溶液中還剩下一種陰離子HCO3-,所以丁溶液中含有HCO3-.
解答 解:A.由②0.1mol•L-1乙溶液中c(H+)>0.1mol•L-1可知乙溶液為多元酸,再根據所給八種離子可知乙溶液為:H2SO4,故A正確;
B.由①甲溶液分別與其它三種溶液混合,均產生白色沉淀,再結合乙溶液為硫酸,可知甲溶液中含有Ba2+,再結合溶液中其他離子可知甲溶液為Ba(OH)2,故B正確;
C.由③向丙溶液中滴入AgNO3溶液,產生不溶于稀HNO3的白色沉淀,可知丙溶液中有Cl-,而丙溶液中的陽離子不能確定,可能是Mg2+,也可能是NH4+,二者的溶液蒸干都不能得到原物質,故C錯誤;
D.溶液中還剩下一種陰離子HCO3-,所以丁溶液中含有HCO3-,故D正確;
故選C.
點評 本題考查了溶液中離子組成的判斷,要結合離子之間的反應,根據現象如:沉淀、氣體等進行判斷.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源: 題型:解答題
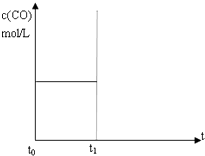 水煤氣(CO 和H2)是重要燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:C (s)+H2O(g)?CO(g)+H2 (g)△H=+131.3kJ•mol-1
水煤氣(CO 和H2)是重要燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:C (s)+H2O(g)?CO(g)+H2 (g)△H=+131.3kJ•mol-1查看答案和解析>>
科目:高中化學 來源: 題型:解答題
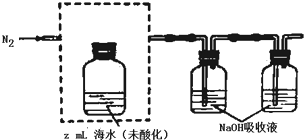
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 研究CO2的利用對促進低碳社會的構建具有重要的意義.
研究CO2的利用對促進低碳社會的構建具有重要的意義.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SiO2不溶于水,也不溶于酸和堿 | B. | SiO2是制造太陽能電池的常用材料 | ||
| C. | 硅是地殼中含量最多的非金屬元素 | D. | 水玻璃可用作木材防火劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋰離子電池放電時電池反應為LiMO2+C6Li1-x═C6Li+Li1-xMO2 | |
| B. | 鋰離子電池充電時電池內部Li+向負極移動 | |
| C. | 鋰離子電池放電時電池內部電流從負極流向正極 | |
| D. | 鋰離子電池充電時陽極反應為C6Li1-x+xLi++xe-═C6Li |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
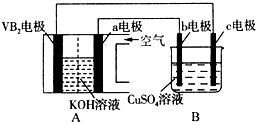 堿性硼化釩(VB2)-空氣電池工作時反應為:4VB2+11O2═4B2O3+2V2O5.用該電池為電源,選用惰性電極電解硫酸銅溶液,實驗裝置如圖所示.當外電路中通過0.04mol電子時,B裝置內共收集到0.448L氣體(標準狀況),則下列說法正確的是( )
堿性硼化釩(VB2)-空氣電池工作時反應為:4VB2+11O2═4B2O3+2V2O5.用該電池為電源,選用惰性電極電解硫酸銅溶液,實驗裝置如圖所示.當外電路中通過0.04mol電子時,B裝置內共收集到0.448L氣體(標準狀況),則下列說法正確的是( )| A. | 電解過程中,c電極表面先有紅色物質析出,然后有氣泡產生 | |
| B. | VB2電極發生的電極反應為:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| C. | 外電路中電子由c電極流向VB2電極 | |
| D. | 若B裝置內的液體體積為200 mL,則CuSO4溶液的物質的量濃度為0.1 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
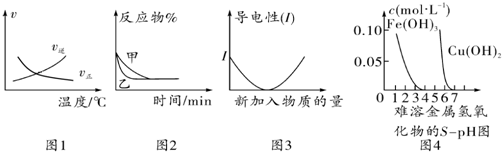
| A. | 根據圖1可判斷可逆反應“A2(g)+3B2(g)?2AB3(g)”的△H<0 | |
| B. | 圖2可能表示壓強對可逆反應 A(g)+2B(g)?3C(g)+D(s)的影響,乙的壓強大 | |
| C. | 圖3可表示乙酸溶液中通入氨氣至過量過程中溶液導電性的變化 | |
| D. | 根據圖4,若除去CuSO4溶液中的Fe3+可采用向溶液中加入適量Cu至pH在4左右 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用容量瓶、量筒、滴定管等儀器時,先用水洗后還需待裝液潤洗 | |
| B. | 洗滌沉淀的操作是將沉淀置于濾紙上(已放置在漏斗中),邊用玻璃棒攪拌邊加蒸餾水沖洗 | |
| C. | 為提升燃料電池的效率,通常可以用KNO3代替蒸餾水,同時作電極的碳棒先灼燒,然后投入到冷水中,反復3-5次 | |
| D. | 在制取乙酸乙酯的實驗中,收集乙酸乙酯的試管中加的是飽和Na2CO3溶液,而且導管直接插入到飽和Na2CO3溶液 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com