
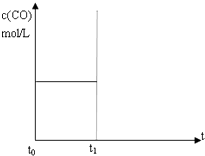
 水煤氣(CO 和H2)是重要燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:C (s)+H2O(g)?CO(g)+H2 (g)△H=+131.3kJ•mol-1
水煤氣(CO 和H2)是重要燃料和化工原料,可用水蒸氣通過熾熱的炭層制得:C (s)+H2O(g)?CO(g)+H2 (g)△H=+131.3kJ•mol-1分析 (1)該反應正反應是吸熱反應,升高溫度平衡向正反應方向移動,據此判斷;
(2)將C全部移走,由于是可逆反應,還會生成碳,生成的碳不能完全反應;
(3)依據平衡標志是正逆反應速率相同,各組分含量保持不變,結合反應特征和平衡移動原理分析選項;
(4)①縮小容器體積,壓強增大,瞬間正反應速率加快,平衡向逆反應移動,正反應速率增大到新平衡;
②降低溫度,瞬間正反應速率減慢,平衡逆反應移動,正反應速率增大到新平衡,據此作圖;
(5)依據化學平衡三段式列式計算,轉化率=$\frac{消耗量}{起始量}$×100%計算得到;
(6)結合熱化學方程式和蓋斯定律計算所需熱化學方程式得到反應焓變.
解答 解:(1)該反應正反應是吸熱反應,升高溫度平衡向正反應方向移動,平衡常數增大;
故答案為:增大;
(2)將C全部移走,由于是可逆反應,還會生成碳,生成的碳不能完全反應,故平衡向左移動,
故答案為:向左移;
(3)C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1 ,反應是氣體體積增大的放熱反應;分析選項正逆反應速率相同是平衡標志;
A.單位體積內每消耗1mol CO的同時生成1molH2 ,說明對一氧化碳或氫氣正逆反應速率相同,故A正確;
B.反應前后氣體物質的量變化,混合氣體總物質的量保持不變說明反應達到平衡狀態,故B正確;
C.生成H2O(g)的速率與消耗CO的速率相等只能說明反應逆向進行,不能說明反應達到平衡狀態,故C錯誤;
D.H2O(g)、CO、H2的濃度相等和起始量變化量有關,不能作為平衡標志,故D錯誤;
故答案為:AB
(4)①縮小容器體積,壓強增大,瞬間正反應速率加快,平衡向逆反應移動,正反應速率增大到新平衡;
②降低溫度,瞬間正反應速率減慢,平衡逆反應移動,正反應速率增大到新平衡,故圖象為: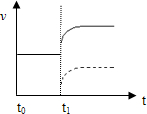 ,故答案為:
,故答案為: ;
;
(5)設H2O轉化了xmol/L,依據化學平衡三段式列式計算;
C (s)+H2O(g)?CO (g)+H2 (g)
初始濃度(mol/L) 2.0 0 0
轉化濃度(mol/L) x x x
平衡濃度(mol/L) 2.0-x x x
達到平衡時測得lgK=-1.0,K=0.1
K=$\frac{{x}^{2}}{2-x}$=1,解得x=1mol/L
所以α(H2O)=$\frac{1mol/L}{2mol/L}$×100%=50%;
故答案為:50%;
(6)①C (s)+H2O(l)?CO(g)+H2(g)△H1
②2CO(g)+O2(g)═2CO2(g)△H2
③H2O(l)═H2 (g)+$\frac{1}{2}$O2(g)△H3
依據蓋斯定律計算①×2+②-2×③得到,C(s)+O2(g)═CO2(g)△H=2△H1+△H2-2△H3;
故答案為:2△H1+△H2-2△H3.
點評 本題考查化學平衡常數及有關計算、化學平衡及反應速率的影響因素、熱化學方程式書寫等,難度中等,(2)是易錯點,學生容易形成定式思維,認為碳是固體,不影響平衡移動,導致錯誤,注意審題是將碳完全移走.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
 某溫度下,在恒容密閉容器中,投入H2(g)和CO2(g),其起始濃度均為0.20mol/L,發生反應:H2(g)+CO2(g)?H2O(g)+CO(g).CO(g)的濃度隨時間變化如圖所示.
某溫度下,在恒容密閉容器中,投入H2(g)和CO2(g),其起始濃度均為0.20mol/L,發生反應:H2(g)+CO2(g)?H2O(g)+CO(g).CO(g)的濃度隨時間變化如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化銫的堿性非常強 | |
| B. | 堿金屬單質中銫的沸點最低 | |
| C. | 將一小塊銫投入水中,實驗現象與鈉和水反應的完全相同 | |
| D. | 銫可以與很多非金屬反應,形成離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溴水中存在下列平衡Br2+H2O?HBr+HBrO,加入AgNO3溶液后,溶液顏色變淺 | |
| B. | 工業上由氫氣和氮氣合成氨是在較高溫度下進行的 | |
| C. | SO2催化氧化成SO3的反應,需要使用催化劑 | |
| D. | H2、I2、HI平衡混和氣加壓后顏色變深 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
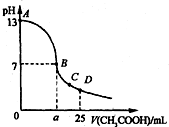 25℃時,在25mL 0.1mol•Lˉ1的NaOH溶液中,逐滴加入0.2mol•Lˉ1的CH3COOH溶液.溶液pH的變化曲線如圖所示.下列分析的結論中,錯誤的是( )
25℃時,在25mL 0.1mol•Lˉ1的NaOH溶液中,逐滴加入0.2mol•Lˉ1的CH3COOH溶液.溶液pH的變化曲線如圖所示.下列分析的結論中,錯誤的是( )| A. | C點時c(CH3COOˉ)>c(Na+)>c(H+)>c(OHˉ) | |
| B. | D點時c(CH3COO-)+c(CH3COOH)=2c(Na+) | |
| C. | 曲線上A、B間任一點,溶液中都有:c(Na+)>c(CH3COOˉ)>c(OHˉ)>c(H+) | |
| D. | B點的橫坐標a>12.5 mL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
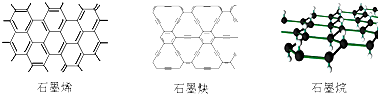
| A. | 石墨烯、石墨炔和石墨烷互為同素異形體 | |
| B. | 12g石墨烯完全轉變為石墨烷需氫氣11.2L | |
| C. | 石墨炔可作半導體材料,有望替代二氧化硅 | |
| D. | 石墨炔孔徑略大于H2分子的直徑,因此它是理想的H2提純薄膜 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
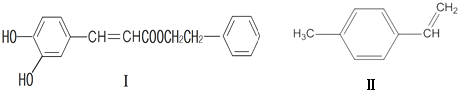
 或
或 (寫1種);由Ⅳ生成Ⅱ的反應條件為NaOH的醇溶液、加熱.
(寫1種);由Ⅳ生成Ⅱ的反應條件為NaOH的醇溶液、加熱.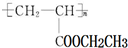 可用于制備涂料,其單體結構簡式為CH2=CHCOOCH2CH3.
可用于制備涂料,其單體結構簡式為CH2=CHCOOCH2CH3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 四種物質中一定有共價化合物 | B. | 四種物質中一定有Ba(OH)2 | ||
| C. | 丙溶液加熱蒸干可得原無水溶質 | D. | 丁溶液中含有HCO3- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com