
| A. | 碳酸氫鈉溶液和稀鹽酸反應:CO32-+2H+═H2O+CO2↑ | |
| B. | 碳酸鉀溶液與稀硫酸反應:CO32-+H+═CO2↑+H2O | |
| C. | 鈉與水反應:2Na+2H2O═2Na++2OH-+H2↑ | |
| D. | 實驗室制取氧氣:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2K++2Cl-+3O2↑ |
分析 A.碳酸氫根離子不能拆開,需要保留整體形式;
B.離子方程式兩邊總電荷不相等;
C.鈉與水反應生成氫氧化鈉和氫氣;
D.氯酸鉀的分解反應不是發生在溶液中的反應,不能書寫離子方程式.
解答 解:A.碳酸氫根離子不能拆開,正確的離子方程式為:HCO3-+H+═H2O+CO2↑,故A錯誤;
B.碳酸鉀溶液與稀硫酸反應的離子方程式為:CO32-+2H+═CO2↑+H2O,故B錯誤;
C.鈉與水反應生成氫氧化鈉和氫氣,反應的離子方程式為:2Na+2H2O═2Na++2OH-+H2↑,故C正確;
D.氯酸鉀的分解反應為:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,該反應不是發生在溶液中的反應,不能書寫離子方程式,故D錯誤;
故選C.
點評 本題考查了離子方程式的判斷,為高考的高頻題,題目難度中等,注意掌握離子方程式的書寫原則,明確離子方程式正誤判斷常用方法,如:檢查反應物、生成物是否正確,檢查各物質拆分是否正確,如難溶物、弱電解質等需要保留化學式,檢查是否符合守恒關系(如:質量守恒和電荷守恒等)等,試題培養了學生的靈活應用能力.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| 物質 | X | Y | Z |
| 初始濃度/mol•L-1 | 0.1 | 0.2 | 0 |
| 2min末濃度/mol•L-1 | 0.08 | a | b |
| 平衡濃度/mol•L-1 | 0.05 | 0.05 | 0.1 |
| A. | 平衡時,X的轉化率為20% | |
| B. | t℃時,該反應的平衡常數為40 | |
| C. | 前2 min內,用Y的變化量表示的平均反應速率v(Y)=0.03 mol•L-1•min-1 | |
| D. | 增大平衡后的體系壓強,v正增大,v逆減小,平衡向正反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②⑤⑥ | B. | ④⑥⑦ | C. | ③④⑦ | D. | 以上都不正確 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
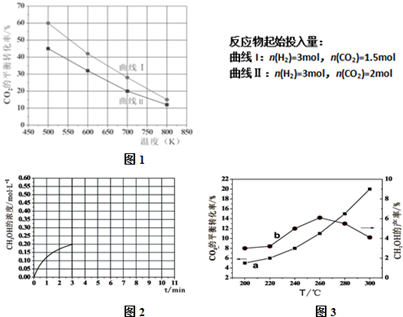
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 的合成路線如圖(部分反應條件省略)
的合成路線如圖(部分反應條件省略)
 (注明反應的條件).
(注明反應的條件). .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
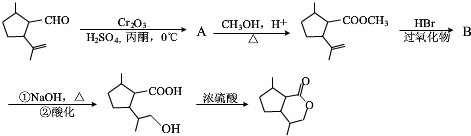
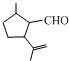 的分子式為C10H16O;其含有的含氧官能團名稱是醛基.
的分子式為C10H16O;其含有的含氧官能團名稱是醛基.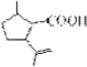 .
. .生成B物質的反應類型為:取代反應.
.生成B物質的反應類型為:取代反應.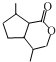 的同分異構體
的同分異構體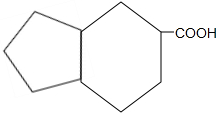 .(任寫一種)
.(任寫一種)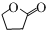 的合成路線圖(無機試劑任選),合成路線流程圖如下:
的合成路線圖(無機試劑任選),合成路線流程圖如下: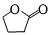
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 (任寫一種).
(任寫一種). 和HCHO為原料制備
和HCHO為原料制備 的合成路線流程圖(無機試劑任用).合成路線流程圖示例如下:
的合成路線流程圖(無機試劑任用).合成路線流程圖示例如下:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com