

分析 (1)A、蒸餾是利用物質沸點不同,控制溫度分離物質,屬于物理變化;
B、煤的干餾是隔絕空氣加強熱,過程中發生復雜物理化學變化;
C、風化是結晶水合物在室溫下失去結晶水的過程;
D、分餾是控制溫度分離不同沸點物質,屬于物理變化;
(2)綠礬是常用的絮凝劑,溶液中亞鐵離子水解生成氫氧化亞鐵,氫氧化亞鐵被空氣中的氧氣氧化生成氫氧化鐵,作為絮凝劑能水解生成膠體凈水,HCO3-會促進絮凝劑中的Fe3+水解,生成更多的膠體;
(3)除去Ca2+、Mg2+,應先加入石灰,然后加入純堿,這樣純堿還可以除去過量的鈣離子;
(4)氯氣和水反應生成次氯酸具有強氧化性能殺死水中的病菌,將CN-氧化成CO2和N2,從而消除CN-的毒性,依據氧化還原反應電子守恒書寫配平離子方程式.
解答 解:(1)A、蒸餾是利用物質沸點不同,控制溫度分離物質,屬于物理變化;
B、煤的干餾是隔絕空氣加強熱,過程中發生復雜物理化學變化;
C、風化是結晶水合物在室溫下失去結晶水的過程,發生了化學變化;
D、分餾是控制溫度分離不同沸點物質,屬于物理變化;
故答案為:BC;
(2)綠礬是常用的絮凝劑,溶液中亞鐵離子水解生成氫氧化亞鐵,氫氧化亞鐵被空氣中的氧氣氧化生成氫氧化鐵,
A.NH4Cl水解顯酸性,不能形成膠體,故A錯誤;
B.食鹽無絮凝劑的作用,故B錯誤;
C.明礬溶液中鋁離子水解形成氫氧化鋁膠體,具有吸附懸浮雜質的作用,故C正確;
D.CH3COONa是強堿弱酸鹽,水解生成醋酸,溶液中無膠體形成,故D錯誤;
若用FeCl3作絮凝劑,實踐中發現廢水中的c(HCO3-)越大,凈水效果越好,原因是HCO3-會促進絮凝劑中的Fe3+水解,生成更多的膠體,凈水效果增強,
故答案為:Fe(OH)3;C;HCO3-會促進絮凝劑中的Fe3+水解,生成更多的膠體,凈水效果增強;
(3)除去Ca2+、Mg2+,應先加入石灰,然后加入純堿,過量的鈣離子可通過純堿使之沉淀下來,此時Ca2+、Mg2+離子分別形成CaCO3、Mg(OH)2沉淀;
故答案為:生石灰;純堿;過量的鈣離子可通過純堿使之沉淀下來;CaCO3,Mg(OH)2;
(4)向濾液2中通人Cl2的作用有兩種:一是利用生成的次氯酸具有強氧化性能殺死水中的病菌;二是將CN-氧化成CO2和N2,從而消除CN-的毒性,若參加反應的C12與CN-的物質的量之比為5:2,Cl2~2Cl-~2e-,2CN-~N2~6e-,CN-~CO2~2e-,則該反應的離子方程式是5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+;
故答案為為:次氯酸;5Cl2+2CN-+4H2O=10Cl-+2CO2+N2+8H+.
點評 本題考查物質的含量測定以及物質的分離、提純實驗方案的設計,題目難度大,注意氧化還原反應原理應用,把握關系式法計算的運用.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1mol•L-1MgCl2溶液中的Mg2+數為nA | |
| B. | 1 mol Na2O2固體中含陰離子總數為2nA | |
| C. | 5 g質量分數為46%的乙醇溶液中,氫原子的總數為0.6 nA | |
| D. | 100 mL 12mol•L-1 濃鹽酸與足量MnO2加熱反應,轉移電子數為1.2nA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將CO2通過Na2O2使其增重a g時,反應中轉移電子數為$\frac{a{N}_{A}}{14}$ | |
| B. | 將1mol Cl2通入到水中,則N(HClO)+N(Cl-)+N(ClO-)=2NA | |
| C. | 常溫常壓下,3.0 g 含甲醛(HCHO)的冰醋酸中含有的原子總數為0.4NA | |
| D. | 2.24L的CH4中含有的C-H鍵數為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | SiHCl3 | SiCl4 | AsCl3 |
| 沸點/℃ | 32.0 | 57.5 | 131.6 |
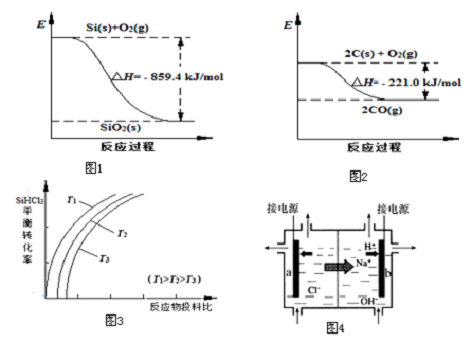
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,1mol氦氣含有的核外電子數為4NA | |
| B. | 常溫常壓下,17g甲基(-14CH3)所含的中子數為8NA | |
| C. | 0.44g C3H8中含有的共用電子對總數目為0.08NA | |
| D. | 常溫常壓下,100 mL 0.5 mol/L 的乙酸溶液中,乙酸的分子數目為0.05NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鎂鋁合金既可完全溶于過量鹽酸又可完全溶于過量NaOH溶液 | |
| B. | 在加入鋁粉能放出氫氣的溶液中,K+、NH4+、CO32-、Cl-一定能夠大量共存 | |
| C. | 氯化鋁溶液中加入過量氨水反應的實質:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 依據鋁熱反應原理,能發生反應2Al+3MgO$\frac{\underline{\;高溫\;}}{\;}$3Mg+A12O3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向碘化亞鐵溶液中通入過量的氯氣:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- | |
| B. | 將少量SO2通入苯酚鈉溶液中:2C6H5O-+SO2+H2O→2C6H5OH+SO32- | |
| C. | 用FeSO4除去酸性廢水中的Cr2O72-:Cr2O72-+Fe2++14H+═2Cr3++Fe3++7H2O | |
| D. | 工業上可用電解法制備Mg:2MgO$\frac{\underline{\;熔融\;}}{電解}$2Mg+O2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com