
分析 N2+3H2?2NH3為可逆反應,既可以從正反應開始,也可以從逆反應開始,不論從哪個方向開始,物質都不能完全反應,N2和H2的化學計量數為1:3,利用極限法假設完全反應,計算出相應物質的濃度變化量,實際變化量小于極限值.
解答 解:若反應向正反應進行到達平衡,假定完全反應,NH3的平衡時物質的量濃度為0.2mol•L-1 ,由方程式N2+3H2?2NH3可知消耗0.1mol•L-1 N2,
則N2 的起始濃度為0.3mol/L,
若反應逆正反應進行到達平衡,假定完全反應,H2的平衡時物質的量濃度為0.3mol•L-1 ,則由方程式N2+3H2?2NH3可知生成0.1mol/L的氮氣,而平衡時氮氣的濃度為0.2moL/L,則起始時為0.1mol/L,
由于為可逆反應,物質不能完全轉化,所以起始時濃度范圍為0.1<c(N2)<0.3,
答:N2 的起始濃度范圍可能是0.1<c(N2)<0.3.
點評 本題考查了可逆反應的特點,題目難度不大,轉移明確可逆反應中反應物轉化率不可能為100%,該題是高考中的常見題型,注重基礎,側重考查學生分析問題、解決問題的能力.


科目:高中化學 來源: 題型:解答題
 物質結構決定物質性質.回答下列問題:
物質結構決定物質性質.回答下列問題: ,其中心原子N的雜化方式是sp3.
,其中心原子N的雜化方式是sp3.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

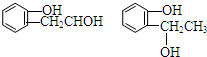 等.①遇FeCl3溶液顯紫色; ②在濃硫酸催化作用下能發生消去反應.
等.①遇FeCl3溶液顯紫色; ②在濃硫酸催化作用下能發生消去反應.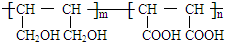 .
.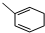 能與CH2=CHCOOH發生類似反應①的反應,生成化合物Ⅷ,寫出Ⅷ的一種結構簡式為
能與CH2=CHCOOH發生類似反應①的反應,生成化合物Ⅷ,寫出Ⅷ的一種結構簡式為 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等物質的量濃度的Na2CO3和NaHCO3混合液中:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| B. | 25℃時 0.2 mol•L-1鹽酸與等體積0.05 mol.L-1Ba(OH)2溶液混合后,溶液的pH=l | |
| C. | 25℃時,pH=3的二元弱酸H2R溶液與pH=ll的NaOH溶液混合后,混合液的pH等于7,則反應后的混合液中:2c(R2-)+c(HR-)=c(Na+) | |
| D. | 25℃時,若0.3 mol.L-1 HY溶液與0.3 mol.L-lNaOH溶液等體積混合后,溶液的pH=9,則:c(OH-)-c(HY)=1×lO-9 mol.L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 3種 | C. | 5種 | D. | 6種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | GFP可以溶于水,且其水溶液可以通過濾紙 | |
| B. | 為了防止GFP變質,可以培養在福爾馬林溶液中 | |
| C. | GFP在一定條件下會發生水解,且水解產物一定只有α-氨基酸 | |
| D. | 灼燒GFP會產生燒焦羽毛的氣味 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
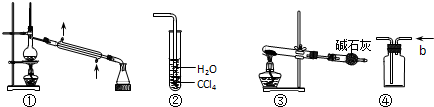
| A. | 裝置①常用于分離某些互溶的液體混合物 | |
| B. | 裝置②可用于吸收HCl氣體,并防止倒吸 | |
| C. | 以NH4HCO3為原料,裝置③可用于實驗室制備少量NH3 | |
| D. | 裝置④b口進氣,可用排空氣法收集H2、NO等氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 制備Al(OH)3懸濁液:向1mol•L-1AlCl3溶液中加過量的6mol•L-1NaOH溶液 | |
| B. | 提純含有少量乙酸的乙酸乙酯:向含有少量乙酸的乙酸乙酯中加入過量飽和Na2CO3溶液,振蕩后靜置分液,并除去有機相的水 | |
| C. | 檢驗溶液中是否含有Fe2+:取少量待檢驗溶液,向其中加入少量新制氯水,再滴加KSCN溶液,觀察實驗現象 | |
| D. | 探究催化劑對H2O2分解速率的影響:在相同條件下,向一支試管中加入2mL5%H2O2和1mLH2O,向另一支試管中加入2mL5%H2O2和1mLFeCl3溶液,觀察并比較實驗現象 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 白鐵(鍍鋅鐵皮)鍍層破損后鐵仍不易腐蝕 | |
| B. | CH3Cl(g)+Cl2(g)$\stackrel{光照}{→}$CH2Cl2(l)+HCl(g)能自發進行,則該反應的△H>0 | |
| C. | MnS懸濁液中滴加少量CuSO4溶液可生成CuS沉淀,則Ksp(CuS)<Ksp(MnS) | |
| D. | 合成氨生產中將NH3液化分離,一定能加快正反應速率,提高H2的轉化率 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com