
| A. | 酸的水溶液呈酸性;則有酸性的水溶液也一定是酸的水溶液 | |
| B. | Fe3O4可寫成FeO?Fe2O3;Pb3O4也可寫成PbO?Pb2O3 | |
| C. | 可電解熔融MgCl2來制取金屬鎂;也能電解熔融HCl來制取氫氣 | |
| D. | 第2周期元素氫化物穩定性順序是HF>H2O>NH3;則第3周期元素氫化物穩定性順序是HCl>H2S>PH3 |
分析 A.氯化銨為強酸弱堿鹽,水解呈酸性;
B.Pb的化合價為+2價、+4價,不存在+3價;
C.氯化氫是共價化合物,熔融HCl不導電;
D.元素的非金屬性越強,其氫化物的穩定性越強.
解答 解:A.氯化銨為強酸弱堿鹽,水解呈酸性,不是酸的水溶液,故A錯誤;
B.Pb的化合價為+2價、+4價,不存在+3價,Pb3O4可表示為2PbO•PbO2,故B錯誤;
C.氯化鎂是離子晶體,可以采用電解熔融氯化鎂的方法冶煉鎂,但是氯化氫是共價化合物,熔融HCl不導電,故C錯誤;
D.元素的非金屬性越強,其氫化物的穩定性越強穩定性順序HF>H2O>NH3、HCl>H2S>PH3,推論正確,故D正確.
故選D.
點評 本題考查了類比思維方法的應用,難度不大,雖然某些物質存在相似性,但也存在差異性,要結合物質的性質來分析移動,易錯選項是C,注意氯化氫是共價化合物是分子晶體而不是離子晶體,為易錯點.


科目:高中化學 來源: 題型:解答題
 如圖1是一套實驗室制取乙烯驗證乙烯具有還原性的實驗裝置,請回答:
如圖1是一套實驗室制取乙烯驗證乙烯具有還原性的實驗裝置,請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molO2與H2的混合氣體中含有的分子數為NA | |
| B. | 1.7g NH3所含原子數為0.1NA | |
| C. | 通常狀況下,11.2L N2中含有的原子數目為NA | |
| D. | 標準狀況下,22.4L H2O中含有的氧原子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
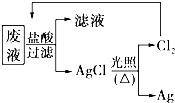 國務院強調“南水北調”工程必須堅持“三先三后”的原則.在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.試分析回答下列問題:
國務院強調“南水北調”工程必須堅持“三先三后”的原則.在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.試分析回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 核磁共振儀、紅外光譜儀、質譜儀、紫外光譜儀、元素分析儀、紫外可見分光光度計等都是定性或定量研究物質組成或結構的現代儀器 | |
| B. | 利用元素周期律,人們在過渡元素中尋找各種性能優良的催化劑,使反應的溫度降低并提高反應物的轉化率,從而起到很好的節能效果 | |
| C. | 淀粉與20%的硫酸混合溶液在沸水浴中充分加熱后滴加碘水無藍色現象,則說明淀粉水解完全 | |
| D. | 分液、蒸餾、滲析、層析及色譜法、鈉融法等都是混合體系分離提純常用的方法 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖是元素周期表的另一種畫法-塔式周期表,在上面標有部分族序數及部分元素,請回答下列問題:
如圖是元素周期表的另一種畫法-塔式周期表,在上面標有部分族序數及部分元素,請回答下列問題:
 或
或
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com