
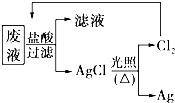
 國務院強調“南水北調”工程必須堅持“三先三后”的原則.在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.試分析回答下列問題:
國務院強調“南水北調”工程必須堅持“三先三后”的原則.在調水工程中,沿途工業污水的任意排放是造成水質惡化的最大隱患.檢測某工廠廢液中,含有大量的Mg2+、Al3+、Cu2+、Ag+.試分析回答下列問題:分析 (1)與Mg2+、Al3+、Cu2+、Ag+中任何離子都不反應的離子可大量共存;
(2)根據氫氧化鋁為兩性氫氧化物的性質進行分離;
(3)n(Ag)=$\frac{108g}{108g/mol}$=1mol,結合反應的關系式2AgCl~Cl2~H2計算.
解答 解:(1)題中SO42-、CO32-、Cl-都可與Ag+反應生產難溶于水或微溶于水的沉淀,只有B符合,故答案為:B;
(2)氫氧化鋁為兩性氫氧化物,可用強堿分離,相關反應的離子方程式為Al3++4OH-=AlO2-+2H2O,
故答案為:Al3++4OH-=AlO2-+2H2O;
(3)n(Ag)=$\frac{108g}{108g/mol}$=1mol,反應的關系式為2AgCl~Cl2~H2,則n(H2)=0.5mol,
V(H2)=0.5mol×22.4L/mol=11.2L,
故答案為:11.2.
點評 本題考查較為綜合,涉及離子共存、離子方程式的書寫及計算,為高考常見題型,側重于學生元素化合物知識的綜合運用,難度不大,注意把握題給信息以及相關離子的性質.


 星級口算天天練系列答案
星級口算天天練系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(NH4+)=c(Na+)=c(OH-)>c(NH3•H2O) | B. | c(NH4+))=c(Na+)>c(NH3•H2O)>c(OH-) | ||
| C. | c(NH4+))>c(Na+)>c(OH-)>c(NH3•H2O) | D. | c(NH4+)>c(Na+)>c(NH3•H2O)>c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②③ | C. | ③① | D. | ①②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 酸的水溶液呈酸性;則有酸性的水溶液也一定是酸的水溶液 | |
| B. | Fe3O4可寫成FeO?Fe2O3;Pb3O4也可寫成PbO?Pb2O3 | |
| C. | 可電解熔融MgCl2來制取金屬鎂;也能電解熔融HCl來制取氫氣 | |
| D. | 第2周期元素氫化物穩定性順序是HF>H2O>NH3;則第3周期元素氫化物穩定性順序是HCl>H2S>PH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2能使品紅溶液褪色 | B. | S在O2中燃燒可生成SO3 | ||
| C. | 用澄清石灰水可鑒別CO2和SO2 | D. | 鈉在氧氣中燃燒生成氧化鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 、④
、④ 、⑤
、⑤ 、⑥
、⑥ .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com