
分析 (1)根據n=$\frac{m}{M}$,V=nVm可知,相同條件下,質量相同時,氣體的相對分子質量越小,氣體所占體積越大;
(2)質量相同時,分子中H元素的質量分數越大,完全燃燒時消耗O2越多;C元素質量分數越大生成二氧化碳越多;
(3)120℃條件下水為氣體,燃燒通式CxHy+(x+$\frac{y}{4}$)O2$\stackrel{點燃}{→}$xCO2+$\frac{y}{2}$H2O(g),完全燃燒前后氣體體積沒有變化,則反應前后氣體總化學計量數不變,據此計算判斷.
解答 解:(1)CH4、C3H4、C2H4、C2H6、C3H6的相對分子質量大小為:CH4<C2H4<C2H6<C3H4<C3H6,根據n=$\frac{m}{M}$,V=nVm可知,相同條件下,質量相同時,氣體的相對分子質量越小,氣體所占體積越大,故質量相同時,在相同狀況下體積最大的是CH4,
故答案為:CH4;
(2)CH4、C3H4、C2H4、C2H6、C3H6的C%大小為:CH4<C2H6<C3H8<C2H4<C2H2,質量相同時,分子中C元素的質量分數越大,完全燃燒時生成CO2越多,故完全燃燒生成CO2最多的是C2H2;故答案為:C2H2;
(3)120℃條件下水為氣體,燃燒通式燃燒通式CxHy+(x+$\frac{y}{4}$)O2$\stackrel{點燃}{→}$xCO2+$\frac{y}{2}$H2O(g),完全燃燒前后氣體體積沒有變化,則1+(x+$\frac{y}{4}$)=x+$\frac{y}{2}$,故y=4,即CH4、C3H4、C2H4完全燃燒后體積不變,
故答案為:CH4、C3H4、C2H4.
點評 本題考查烴燃燒耗氧量、生成二氧化碳與水的量問題,難度不大,注意對規律的理解與掌握.


 培優口算題卡系列答案
培優口算題卡系列答案 開心口算題卡系列答案
開心口算題卡系列答案 口算題卡河北少年兒童出版社系列答案
口算題卡河北少年兒童出版社系列答案科目:高中化學 來源: 題型:解答題
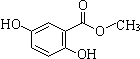
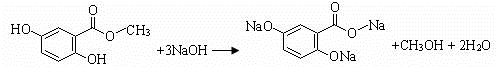 .(不用寫反應條件)
.(不用寫反應條件)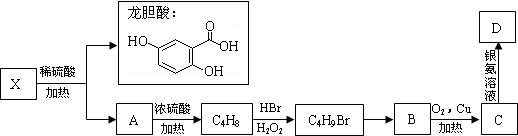
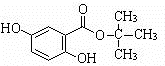 .
.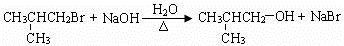 .(用結構簡式表示)
.(用結構簡式表示)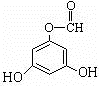 或
或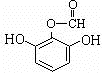 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用藥匙取用粉末狀或小顆粒狀固體 | |
| B. | 用膠頭滴管滴加少量液體 | |
| C. | 給盛有2/3體積液體的試管加熱 | |
| D. | 過濾時漏斗的下端管口要緊靠燒杯內壁 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | V1=10V2 | B. | V1>10V2 | C. | V1<10V2 | D. | V2>10V1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 人工腎臟可用間接電化學方法除去代謝產物中的尿素(CO(NH2)2),原理如圖.
人工腎臟可用間接電化學方法除去代謝產物中的尿素(CO(NH2)2),原理如圖.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 Na2O2與水的反應實際是Na2O2+2H2O═2NaOH+H2O2,反應放出的熱量使部分H2O2受熱分解:2H2O2═2H2O+O2↑.為了測定某過氧化鈉固體的純度,今做如下實驗:
Na2O2與水的反應實際是Na2O2+2H2O═2NaOH+H2O2,反應放出的熱量使部分H2O2受熱分解:2H2O2═2H2O+O2↑.為了測定某過氧化鈉固體的純度,今做如下實驗:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度(k) CO2轉化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com