
 (1)根據要求填空:
(1)根據要求填空:
分析 (1)a.Cu元素原子核外電子數為29,根據能量最低原理書寫核外電子排布式;
b.MgCl2由鎂離子與氯離子構成;
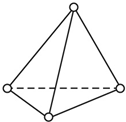
(2)a.P4分子為正四面體型分子,每個面為正三角形;
b.P4分子中有6個P-P鍵;
c.P4分子為對稱結構,屬于非極性分子;
(3)中心原子或離子提供空軌道,配體提供孤電子對.
解答 解:(1)a.Cu元素原子核外電子數為29,核外電子排布式為[Ar]3d104s1,故答案為:[Ar]3d104s1;
b.MgCl2由鎂離子與氯離子構成,電子式為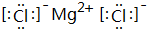 ,故答案為:
,故答案為: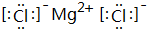 ;
;
(2)a.P4分子為正四面體型分子,每個面為正三角形,分子中P-P鍵之間的夾角為60°,故答案為:60°;
b.P4分子中有6個P-P鍵,1mol P4分子中有6mol P-P鍵,故答案為:6;
c.P4分子為對稱結構,屬于非極性分子,故答案為:非極性;
(3)a.[Ag(NH3)2]+的中心離子為Ag+,配體為NH3,故答案為:NH3;
b.[AlF6]3-:的中心離子為Al3+,配體為F-,故答案為:F-.
點評 本題考查核外電子排布、電子式、分子結構、化學鍵、配合物等,注意對基礎知識的理解掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
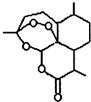 合理使用藥物是保證身心健康、提高生活質量的有效手段.藥物化學已經成為化學的一個重要領域.
合理使用藥物是保證身心健康、提高生活質量的有效手段.藥物化學已經成為化學的一個重要領域.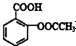 是常用的解熱鎮痛藥,可以由水楊酸與乙酸酐反應制取,反應原理為:
是常用的解熱鎮痛藥,可以由水楊酸與乙酸酐反應制取,反應原理為: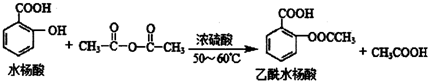
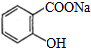 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在常溫下,0.10mol•L-1Na2CO3溶液25mL 用0.10mol•L-1鹽酸滴定.當滴定到消耗20mlHCl時所得溶液中離子濃度間的關系有:5c(Cl-)=4c(HCO3-)+4c(CO32-)+4c(H2CO3) | |
| B. | 常溫下,pH=12的氨水與pH=2的鹽酸等體積混合溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| C. | 25℃時,0.1 mol•L-1pH=4.5的NaHSO3溶液中:c(HSO3-)>c(H2SO3)>c(SO32-) | |
| D. | 常溫下,等濃度的CH3COONa和CH3COOH混合溶液:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 因為稀硫酸能與鐵反應放出H2,所以稀硝酸與鐵反應也一定能放出H2 | |
| B. | 因為Mg可以與水反應放出H2,所以Ca也可以與水反應放出H2 | |
| C. | 因為CO2的水溶液可以導電,所以CO2是電解質 | |
| D. | 因為SO2可以使酸性KMnO4溶液褪色,所以SO2具有漂白性 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
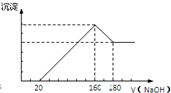 將一定質量的鎂鋁合金投入100mL一定濃度的鹽酸中,合金完全溶解.向所得溶液中滴加濃度為5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的體積關系如圖.(橫坐標體積單位是mL,縱坐標質量單位是g)
將一定質量的鎂鋁合金投入100mL一定濃度的鹽酸中,合金完全溶解.向所得溶液中滴加濃度為5mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的體積關系如圖.(橫坐標體積單位是mL,縱坐標質量單位是g) 查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com