
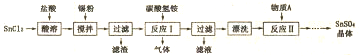
分析 SnCl2能水解生成堿式氯化亞錫,用鹽酸溶解,防止其水解,在酸性條件下,溶液中的Sn2+可被空氣中的氧氣氧化成Sn4+,加入錫粉主要是防止在溶解時被空氣中氧氣氧化,過濾出錫粉,得到SnCl2溶液,(4)中反應Ⅰ與碳酸氫銨反應生成SnO,Sn元素化合價未變化,屬于非氧化還原反應,同時生成氣體,該氣體為二氧化碳,發生反應:SnCl2+2NH4HCO3═SnO↓+2CO2↑+2NH4Cl+H2O,溫度較高時碳酸氫銨會分解,需要控制在75℃左右.過濾得到SnO,洗滌表面附著的NH4Cl等,進行洗滌,再利用SnO與硫酸反應得到SnSO4溶液,經過蒸發濃縮、冷卻結晶等操作得到SnSO4是晶體.
(1)錫原子的核電荷數為50,與碳元素屬于同一主族,處于ⅣA族,根據原子序數減各周期容納元素種數確定所在的周期;
(2)由信息可知,SnCl2易水解生成堿式氯化亞錫,加入鹽酸,抑制Sn2+水解;
(3)由信息可知,Sn2+易被氧化,加入Sn粉除調節溶液pH外,還防止Sn2+被氧化;
(4)反應Ⅰ得到沉淀是SnO,Sn元素化合價未變化,屬于非氧化還原反應,同時生成氣體,該氣體為二氧化碳;由于碳酸氫銨容易分解,需要控制在75℃左右;
(5)SnO表面附著的NH4Cl等,用AgNO3溶液檢驗最后一次洗滌液是否含有氯離子,判斷是否洗滌干凈;
(6)潮濕環境中,Sn與Cu構成原電池,Sn作為負極,保護正極Cu不被氧化.
解答 解:SnCl2能水解生成堿式氯化亞錫,用鹽酸溶解,防止其水解,在酸性條件下,溶液中的Sn2+可被空氣中的氧氣氧化成Sn4+,加入錫粉主要是防止在溶解時被空氣中氧氣氧化,過濾出錫粉,得到SnCl2溶液,(4)中反應Ⅰ與碳酸氫銨反應生成SnO,Sn元素化合價未變化,屬于非氧化還原反應,同時生成氣體,該氣體為二氧化碳,發生反應:SnCl2+2NH4HCO3═SnO↓+2CO2↑+2NH4Cl+H2O,溫度較高時碳酸氫銨會分解,需要控制在75℃左右.過濾得到SnO,洗滌表面附著的NH4Cl等,進行洗滌,再利用SnO與硫酸反應得到SnSO4溶液,經過蒸發濃縮、冷卻結晶等操作得到SnSO4是晶體.
(1)錫元素與碳元素屬于同一主族,處于ⅣA族,原子核電荷數為50,則:50-2-8-8-18=14,故Sn處于第五周期,則在周期表中的位置為:第五周期第ⅣA族,
故答案為:五;
(2)由信息可知,SnCl2易水解生成堿式氯化亞錫,存在平衡Sn Cl2+H2O?Sn(OH)Cl+HCl,加入鹽酸,使該平衡向左移動,抑制Sn2+水解,
故答案為:SnCl2+H2O?Sn(OH)Cl+HCl;
(3)由信息可知,Sn2+易被氧化,加入Sn粉除調節溶液pH外,還除去酸溶時產生的少量Sn4+、防止Sn2+被氧化,
故答案為:除去酸溶時產生的少量Sn4+、防止Sn2+被氧化;
(4)反應Ⅰ得到沉淀是SnO,Sn元素化合價為變化,屬于非氧化還原反應,同時生成氣體,該氣體為二氧化碳,反應方程式為:SnCl2+2NH4HCO3═SnO↓+2CO2↑+2NH4Cl+H2O,溫度較高時碳酸氫銨會分解,該反應的溫度需要控制在75℃左右,
故答案為:SnCl2+2NH4HCO3═SnO↓+2CO2↑+2NH4Cl+H2O;溫度較高時碳酸氫銨會分解;
(5)SnO表面附著的NH4Cl等,檢驗沉淀已經“漂洗”干凈的方法:取少量最后一次洗滌液于試管中,滴入幾滴AgNO3溶液,若無白色沉淀生成,則說明沉淀已洗滌干凈;
A與SnO反應得到SnSO4溶液,故A為硫酸,
故答案為:取少量最后一次洗滌液于試管中,滴入幾滴AgNO3溶液,若無白色沉淀生成,則說明沉淀已洗滌干凈;硫酸;
(6)潮濕環境中,Sn與Cu構成原電池,Sn作為負極,保護正極Cu不被氧化,故即使錫層破損也能防止形成銅綠,
故答案為:潮濕環境中,Sn與Cu構成原電池,Sn作為負極,保護正極Cu不被氧化.
點評 本題考查制備實驗方案,涉及對工藝流程的理解、對操作的分析評價、物質的分離提純、金屬腐蝕與防護、閱讀題目獲取信息的能力等,是對學生綜合能力的考查,難度中等.


科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 實驗結論 |
(1)A的質譜圖如下: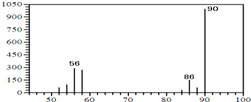 | (1)證明A的相對分子質量為90. |
| (2)將此9.0g A在足量純O2充分燃燒,并使其產物依次緩緩通過濃硫酸、堿石灰,發現分別增重5.4g和13.2g. | (2)證明A的分子式為: C3H6O3. |
| (3)另取兩份9.0g A分置于不同的試管中.往其中一份A中加入足量的NaHCO3粉末充分反應,生成2.24 L CO2(標準狀況). 往另一份A中加入足量金屬鈉充分反應,生成2.24 L H2(標準狀況). | (3)證明A的分子中含有羧基和羥基官能團. |
(4)A的核磁共振氫譜如圖: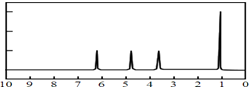 | (4)A的結構簡式為: . . |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氣體擴散速率與擴散面積成正比 | |
| B. | 氣體擴散速率與氣體溶解度和分子量成正比 | |
| C. | 氣體擴散速率與分壓差成正比 | |
| D. | 氣體擴散速率與溫度成正比 | |
| E. | 氣體擴散速率與擴散距離成反比 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 與
與
 與
與
 與
與
 與
與
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 測試時間段 | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
| 序號 | 二氧化硫的性質 | 主要操作和現象 | 化學方程式 |
| ① | 將二氧化硫通入裝有品紅溶液的 試管中,品紅由紅色變為無色 | ||
| ② | 將二氧化硫與硫化氫氣體混合,出現 黃色固體. | SO2+2H2S=3S+2H2O | |
| ③ | 將二氧化硫通入裝有新制氯水的試管中,氯水由淺黃綠色變為無色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com