
【題目】I.甲醛在木材加工、醫藥等方面有重要用途。甲醇直接脫氫是工業上合成甲醛的新方法,制備過程涉及的主要反應如下:
反應I:CH3OH(g)![]() HCHO(g)+H2(g) △H1=+85.2kJ/mol
HCHO(g)+H2(g) △H1=+85.2kJ/mol
反應II:CH3OH(g)+![]() O2(g)
O2(g)![]() HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
反應III:2H2(g)+O2(g)![]() 2H2O(g) △H3=-483.6kJ/mol
2H2O(g) △H3=-483.6kJ/mol
(1)計算反應Ⅱ的反應熱△H2=_____________________________。
(2)750K下,在恒容密閉容器中,發生反應CH3OH(g)![]() HCHO(g)+H2(g),若起始壓強為P0,達到平衡轉化率為α,則平衡時的總壓強P平=___________(用含P0和α的式子表示);當P0=101kPa,測得α=50.0%,計算反應平衡常數Kp=___________kPa(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數,忽略其它反應)。
HCHO(g)+H2(g),若起始壓強為P0,達到平衡轉化率為α,則平衡時的總壓強P平=___________(用含P0和α的式子表示);當P0=101kPa,測得α=50.0%,計算反應平衡常數Kp=___________kPa(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數,忽略其它反應)。
II.CO2既是溫室氣體,也是重要的化工原料,以CO2為原料可合成多種有機物。
(3)CO2用于生產乙烯,已知:2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定條件下,按不同的投料比X[X=
CH2=CH2(g)+4H2O(g) △H=QkJ/mol。一定條件下,按不同的投料比X[X=![]() ]向某容積可變的恒壓密閉容器中充入CO2、H2,測得不同投料比時CO2的轉化率與溫度的關系如圖所示。
]向某容積可變的恒壓密閉容器中充入CO2、H2,測得不同投料比時CO2的轉化率與溫度的關系如圖所示。

①X1_____X2(填“>”或“<”,后同),Q_____0。
②圖中A、B、C三點對應的平衡常數KA、KB、KC的大小關系為_____。
(4)常溫下,用NaOH溶液作CO2捕捉劑不僅可以降低碳排放,而且可得到重要的化工產品Na2CO3。
①若某次捕捉后得到pH=10的溶液,則溶液中c(CO32-):c(HCO3-)=_____[常溫下K1(H2CO3)=4.4×10﹣7、K2(H2CO3)=5×10﹣11]。
②欲用5L Na2CO3溶液將23.3g BaSO4固體全都轉化為BaCO3,則所用的Na2CO3溶液的物質的量濃度至少為__________。[已知:常溫下Ksp(BaSO4)=1×10﹣7、Ksp(BaCO3)=2.5×10﹣6]。(忽略溶液體積積的變化)
【答案】-156.6kJ/mol P0(1+α) 50.5 > < KA>KB=KC 1:2 0.52mol/L
【解析】
(1)根據蓋斯定律,反應I+![]() 反應III得反應Ⅱ,據此計算△H2;
反應III得反應Ⅱ,據此計算△H2;
(2)根據恒容時氣體的壓強比等于氣體的物質的量的比計算平衡時的壓強;根據平衡常數表達式計算其平衡常數;
(3)①當其他條件一定時,充入的H2量越多,CO2轉化率越高,對應的X越大,則X1>X2;在其它條件不變時,結合圖象可知:溫度升高,CO2的轉化率降低,可推知該反應的正反應是放熱反應,據此進行分析;
②結合圖象可知該反應正反應為放熱反應,則溫度升高,化學平衡常數將減小,而且化學平衡常數只與溫度有關;
(4)①由題意pH=10,可計算c(H+)=1×10-10mol/L,由HCO3-![]() CO32-+H+可得:Ka2=
CO32-+H+可得:Ka2=![]() =5×10﹣11,所以
=5×10﹣11,所以![]() =1:2;
=1:2;
②設至少需要物質的量濃度為xmol/L的Na2CO3溶液,當BaSO4完全溶解后,23.3g BaSO4的物質的量為n(BaSO4)= 23.3g÷233g/mol=0.1mol,所得5L溶液中c(SO42-)=0.1mol ÷5L=0.02mol/L,此時溶液中c(CO32-)=(x-0.02)mol/L,由BaSO4+CO32-=BaCO3+SO42-可知,此反應的化學平衡常數K=![]() =0.04=
=0.04=![]() ,據此進行計算。
,據此進行計算。
(1)I+![]() ×III,整理可得CH3OH(g)+
×III,整理可得CH3OH(g)+![]() O2(g)
O2(g)![]() HCHO(g)+H2O(g) △H2=△H1+
HCHO(g)+H2O(g) △H2=△H1+![]() ×△H3=-156.6kJ/mol;
×△H3=-156.6kJ/mol;
(2)根據在恒容時氣體的壓強比等于氣體的物質的量的比計算平衡時的壓強。若起始壓強為P0,達到平衡轉化率為α,
CH3OH(g)![]() HCHO(g)+H2(g)
HCHO(g)+H2(g)
起始(mol) 1 0 0
變化(mol) a a a
平衡(mol) 1-a a a
壓強之比等于物質的量之比,則p0:P平=1(1+a),P平=p0(1+a)。當P0=101kPa,測得α=50.0%,該反應平衡常數Kp=![]() =50.5 kPa;
=50.5 kPa;
(3)①當其他條件一定時,充入的H2量越多,CO2轉化率越高,對應的X越大,則X1>X2;在其它條件不變時,結合圖象可知:溫度升高,CO2的轉化率降低,可推知該反應的正反應是放熱反應,則Q<0;
②結合圖象可知該反應的正反應為放熱反應。溫度升高,平衡逆向移動,該反應的化學平衡常數減小;而且化學平衡常數只與溫度有關,根據圖象知A點的溫度低于B、C兩點,而且B、C兩點溫度相同,則三點對應的平衡常數的大小關系為:KA>KB=KC;
(4)①)①由題意pH=10,可計算c(H+)=1×10-10mol/L,由HCO3-![]() CO32-+H+可得:Ka2=
CO32-+H+可得:Ka2=![]() =5×10﹣11,所以
=5×10﹣11,所以![]() =1:2;
=1:2;
②設至少需要物質的量濃度為xmol/L的Na2CO3溶液,當BaSO4完全溶解后,23.3g BaSO4的物質的量為n(BaSO4)= 23.3g÷233g/mol=0.1mol,所得5L溶液中c(SO42-)=0.1mol ÷5L=0.02mol/L,此時溶液中c(CO32-)=(x-0.02)mol/L,由BaSO4+CO32-=BaCO3+SO42-可知,此反應的化學平衡常數K=![]() =0.04=
=0.04=![]() ;
;
②設至少需要物質的量濃度為xmol/L的Na2CO3溶液,當BaSO4完全溶解后,所得5L溶液中c(SO42-)=0.02mol/L,此時溶液中c(CO32-)=(x-0.02)mol/L,由BaSO4+CO32-=BaCO3+SO42-可知,此反應的化學平衡常數K=![]() =0.04=
=0.04=![]() ,解得x=0.52mol/L。
,解得x=0.52mol/L。


 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案科目:高中化學 來源: 題型:
【題目】為應對全球石油資源口益緊缺。提高煤的利用效率,我國開發了煤制烴技術,并進入工業化試驗階段。
(1)煤氣化制合成氣(CO和H2):C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ/mol該反應在高溫下能自發進行,理由是_____________。
(2)由合成氣制甲醇:合成氣CO和H2在一定條件下能發生如下反應:
主反應I.CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
反應II.CO(g)+H2(g)![]() C(s)+H2O(g)
C(s)+H2O(g)
①在容積均為VL的甲、乙、丙三個密閉容器中分別充入amolCO和2 amolH2,三個容器的反應溫度分別為T1、T2、T3(T1<T2<T3)且恒定不變,若只發生反應I,在其他條件相同的情況下,實驗測得反應均進行到tmin時CO的體積分數如圖所示,此時三個容器中一定處于化學平衡狀態的是_____(填“T1”、“T2”或“T3”):該溫度下的化學平衡常數為_____(用a、V表示)。

②為減弱副反應的發生,下列采取的措施合理的是______。
A.反應前加入少量的水蒸氣 B.增壓
C.降低反應溫度 D.使用合適催化劑,提高甲醇的選擇性
(3)由甲醇制烯烴
主反應:i.2CH3OH![]() C2H4+2H2O
C2H4+2H2O
ii.3CH3OH![]() C3H6+3H2O
C3H6+3H2O
副反應:iii.2CH3OH![]() CH3OCH3+H2O
CH3OCH3+H2O
某實驗室控制反應溫度為400℃,在相同的反應體系中分別填裝等量的兩種催化劑(Cat.1和Cat.2),以恒定的流速通入CH3OH,在相同的壓強下進行兩種催化劑上甲醇制烯烴的對比研究。得到如圖實驗數據:(選擇性:轉化的甲醇中生成乙烯和丙烯的百分比)


下列說法不正確的是_________。
A.反應進行一段時間后甲醇的轉化率減小,可能的原因是催化劑失活,工業生產中需定期更換催化劑
B.使用Cat.2反應2h后乙烯和內烯的選擇性下降,可能的原因是生成副產物二甲醚
C.使用Cat.1產生的烯烴主要為丙烯,使用Cat.2產生的烯烴主要為乙烯
D.不管使用Cat.1還是使用Cat.2都能提高活化分子的百分數
(4)已知:2CrO42-+2H+![]() Cr2O72-+H2O。以鉻酸鉀為原料,電化學法備重鉻酸鉀的實驗裝置示意圖如下
Cr2O72-+H2O。以鉻酸鉀為原料,電化學法備重鉻酸鉀的實驗裝置示意圖如下

①a為電源的________(填“正極”或“負極”)
②該制備過程總反應的化學方程式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按如圖所示裝置進行實驗,并回答下列問題。

⑴銅片上的現象是__________________________ ,電極反應為________________ ,_____________(填“鋅片”或“銅片”)只起傳導電子的作用。
⑵電子由_____________經導線流向_____________ ,_____________為負極。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面是第二周期部分元素基態原子的電子排布圖,據此下列說法錯誤的是( )


A. 每個原子軌道里最多只能容納2個電子
B. 電子排在同一能級時,總是優先單獨占據一個軌道
C. 每個能層所具有的能級數等于能層的序數(n)
D. 若原子軌道里有2個電子,則其自旋狀態相反
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示是一種以液態肼(N2H4)為燃料,氧氣為氧化劑,某固體氧化物為電解質的新型燃料電池。該固體氧化物電解質的工作溫度高達700~900℃時,O2-可在該固體氧化物電解質中自由移動,反應生成物均為無毒無害的物質。下列說法正確的是

A. 電池總反應為:N2H4+2O2=2NO+2H2O
B. 電池內的O2-由電極乙移向電極甲
C. 當甲電極上有lmol N2H4消耗時,乙電極上有22.4LO2參與反應
D. 電池正極方程式為:O2 + 4e-+2H2O=4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】O3能吸收有害紫外線,保護人類賴以生存的空間。O3的分子結構如圖,呈V形,兩個鍵的夾角為116.5°,三個原子以一個O原子為中心,與另外兩個O原子分別構成一個共價鍵;中間O原子提供兩個電子,旁邊兩個O原子各提供一個電子,構成一個特殊的化學鍵——三個O原子均等地享有這些電子。請回答:

(1)臭氧與氧氣互為________________。
(2)下列分子與O3分子的結構最相似的是________。
A. H2O B. CO2 C. SO2 D. BeCl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于化學觀或化學研究方法的敘述中,錯誤的是( )
A. 在化工生產中應遵循“綠色化學”的思想
B. 在過渡元素中尋找優良的催化劑
C. 在元素周期表的金屬和非金屬分界線附近尋找半導體材料
D. 根據元素周期律,由HClO4可以類推出氟元素的最高價氧化物的水化物為HFO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業鍋爐內壁的水垢,不僅浪費燃料,而且容易引發安全隱患。某碳素鋼鍋爐水垢(主要成分有CaCO3、CaSO4、Mg(OH)2、Fe2O3、SiO2等)堿煮法清除的流程如下:

已知:20℃時幾種難溶物的溶度積常數如下表(單位省略):

回答下列問題:
(1)“堿煮”環節,加入Na3PO4的主要目的是將CaSO4轉化為Ca3(PO4)2,請寫出該離子方程式______________________。
(2)“浸泡過程中,稀鹽酸會溶解Fe2O3。溶解后的Fe2O3會加速鍋爐腐蝕,故需“還原”處理。
①鍋爐被加速腐蝕的原因是______________________;
②浸泡液還原”處理時,Sn2+轉化為Sn4+,則反應中氧化劑與還原劑的物質的量之比為______________________。
(3)“鈍化”處理的目的是在鍋爐表面形成Fe3O4保護膜,同時生成可直接參與大氣循環的氣體。
①反應的離子方程式為_________________________________;
②為檢驗鍋爐“鈍化”處理后是否形成致密的保護膜,可往鍋爐內壁刷上硫酸銅溶液。若觀察到______________________(填現象),則保護膜致密性欠佳。
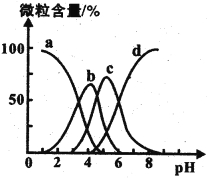
(4)檸檬酸(用H3R表示)可用作清除鍋爐水垢的酸洗劑,溶液中H3R、H2R-、HR2-、R3-的含量與pH的關系如圖所示。由此可推知,0.1 mol ·L-1 Na2HR溶液中各種陰離子濃度由大到小的排列順序為______________________。
(5)用如圖裝置對鍋爐用水(含Ca2+、Mg2+、HCO3-)進行預處理,可有效防止水垢形成。電解時,Ca2+形成沉淀的電極反應式為______________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究含碳化合物的結構與性質,對生產、科研等具有重要意義
(1)冠醚是由多個二元醇分子之間失水形成的環狀化合物。X、Y、Z是常見的三種冠醚,其結構如圖所示。它們能與堿金屬離子作用,并且隨著環的大小不同而與不同金屬離子作用。

①Li+計與X的空腔大小相近,恰好能進入到X的環內,且Li+與氧原子的一對孤電子對作用形成穩定結構W(如圖)。
a.基態鋰離子核外能量最高的電子所處能層符號為___________;
b.W中Li+與孤對電子之間的作用屬于___________(選填字母標號)
A.離子鍵 B.共價鍵 C.配位鍵 D.氫鍵 E.以上都不是
②冠醚Y能與K+形成穩定結構,但不能與Li+計形成穩定結構。理由是___________。
③烯烴難溶于水,被KMnO4水溶液氧化的效果較差。若烯烴中溶人冠醚Z,氧化效果明顯提升。
i.水分子中氧的雜化軌道的空間構型是___________,H-O鍵鍵角___________(填“>”“<”或“=”)109°28′
ii.已知:冠醚Z與KMnO4可以發生右圖所示的變化。加入冠醚Z后,烯烴的氧化效果明顯提升的原因是___________。
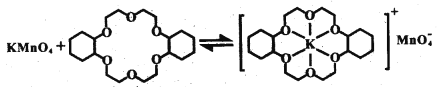
(2)甲烷是重要的清潔能源,其晶體結構如圖所示,晶胞參數為anm。
①常溫常壓下不存在甲烷晶體。從微粒間相互作用的角度解釋,其理由是___________;
②甲烷分子的配位數為___________;
③A分子中碳原子的坐標參數為(0,0,0),則B分子的碳原子的坐標參數為___________。
④甲烷晶體的密度為___________(g·cm-3)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com