
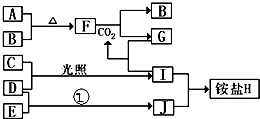
 如圖是部分短周期元素的單質及其化合物(或其溶液)的轉化關系,已知B、C、D、E是非金屬單質且在常溫常壓下都是氣體;化合物G的焰色反應為黃色,化合物I和J通常狀況下呈氣態;反應①是化工生產中的一種固氮反應.
如圖是部分短周期元素的單質及其化合物(或其溶液)的轉化關系,已知B、C、D、E是非金屬單質且在常溫常壓下都是氣體;化合物G的焰色反應為黃色,化合物I和J通常狀況下呈氣態;反應①是化工生產中的一種固氮反應.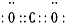 .
. 2NH3的化學方程式.
2NH3的化學方程式.分析 化合物G的焰色反應為黃色,含有Na元素,F能與二氧化碳反應得到氣體單質B與G,可推知F為Na2O2,B為O2,G為Na2CO3,而A與B(氧氣)反應得到F(過氧化鈉),則A為Na.G(Na2CO3)與I反應得到CO2,則I屬于酸,I由氣體非金屬單質C與D在光照條件下得到,則I為HCl,C、D分別為H2、Cl2中的一種,I和J通常狀況下呈氣態,二者反應得到銨鹽,且反應①是化工生產中的一種重要固氮反應,可推知J為NH3,D為H2,E為N2,銨鹽為NH4Cl,故C為Cl2,據此解答.
解答 解:化合物G的焰色反應為黃色,含有Na元素,F能與二氧化碳反應得到氣體單質B與G,可推知F為Na2O2,B為O2,G為Na2CO3,而A與B(氧氣)反應得到F(過氧化鈉),則A為Na,G(Na2CO3)與I反應得到CO2,則I屬于酸,I由氣體非金屬單質C與D在光照條件下得到,則I為HCl,C、D分別為H2、Cl2中的一種,I和J通常狀況下呈氣態,二者反應得到銨鹽,且反應①是化工生產中的一種重要固氮反應,可推知J為NH3,D為H2,E為N2,銨鹽為NH4Cl,C為Cl2,
(1)由上述分析可知,H的化學式為NH4Cl,CO2的電子式為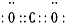 ,
,
故答案為:NH4Cl;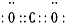 ;
;
(2)A和B反應方程式為:2Na+O 2$\frac{\underline{\;點燃\;}}{\;}$ Na2O2,
D和E的反應方程式為:N2+3H2 2NH3,
2NH3,
故答案為:2Na+O 2$\frac{\underline{\;點燃\;}}{\;}$ Na2O2;N2+3H2 2NH3;
2NH3;
(3)化合物G與I反應的離子方程式:2 H++CO32-═CO2+H2O,
故答案為:2 H++CO32-═CO2+H2O;
(4)F和CO2的化學方程式為:2Na2O2+2CO2═2Na2CO3+O2,
故答案為:2Na2O2+2CO2═2Na2CO3+O2.
點評 本題考查無機物推斷,涉及Na、Cl、N元素單質化合物性質,物質的狀態、焰色反應及轉化中特殊反應等是推斷突破口,側重基礎知識的鞏固,難度不大,注意中學常見化學工業.


 應用題天天練四川大學出版社系列答案
應用題天天練四川大學出版社系列答案科目:高中化學 來源: 題型:解答題
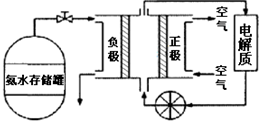
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用無毒無害的原料 | B. | 使用顏色為綠色的化工產品 | ||
| C. | 不使用任何化學物質 | D. | 使用不可再生的資源 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 電池負極反應為:Zn-2e-═Zn2+ | B. | 鋅是負極,碳棒是正極 | ||
| C. | 電子由碳棒經外電路流向鋅 | D. | 鋅錳干電池屬一次電池 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 有A、B、C、D四種元素,其中A元素和B元素的原子都有1個未成對電子,A+比B-少一個電子層,B原子得一個電子后3p軌道全滿;C原子的p軌道中有3個未成對電子,其氣態氫化物在水中的溶解度在同族元素所形成的氫化物中最大;D的最高化合價和最低化合價的代數和為4,其最高價氧化物中含D的質量分數為40%,且其核內質子數等于中子數.R是由A、D兩元素形成的離子化合物,其中A與D離子數之比為2:1.請回答下列問題:
有A、B、C、D四種元素,其中A元素和B元素的原子都有1個未成對電子,A+比B-少一個電子層,B原子得一個電子后3p軌道全滿;C原子的p軌道中有3個未成對電子,其氣態氫化物在水中的溶解度在同族元素所形成的氫化物中最大;D的最高化合價和最低化合價的代數和為4,其最高價氧化物中含D的質量分數為40%,且其核內質子數等于中子數.R是由A、D兩元素形成的離子化合物,其中A與D離子數之比為2:1.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下反應4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)的△H>0,△S<0 | |
| B. | 500℃、30 MPa下,將0.5 mol N2和1.5 mol H2置于密閉容器中充分反應,放熱19.3 kJ,其熱化學方程式為:N2(g)+3H2(g)$?_{500℃、30MPa}^{催化劑}$2NH3(g),△H=-38.6 kJ•mol-1 | |
| C. | FeCl3溶液中通入SO2,溶液黃色褪去:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ | |
| D. | 向苯酚鈉溶液中通入CO2,溶液變渾濁:2C6H5O-+CO2+H2O-→2C6H5OH↓+CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
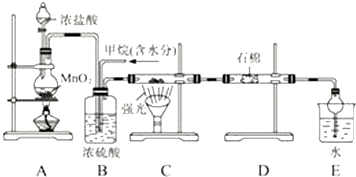
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
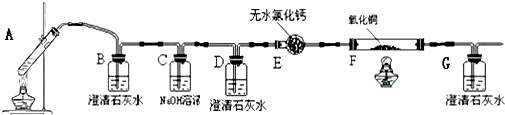
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com