
【題目】以煉鋅廠的煙道灰(主要成分為ZnO,另含少量Fe2O3、CuO、SiO2、MnO等)為原料可生產草酸鋅晶體(ZnC2O42H2O)
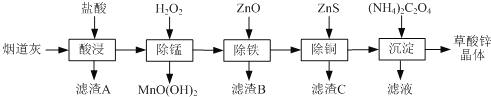
已知:常溫下Ksp[Fe(OH)3]=2.6×10-39, Ksp[Cu(OH)2]=2.2×10-20。
請問答下列問題:
(1)為了提高“酸浸”時鋅元素的浸出率,可以采取的措施有:_________、________(填寫2條)。
(2)“除錳”反應后,溶液的pH__________(填“增大”“減小”或“不變”)。
(3)常溫下“除鐵”反應中,加入ZnCO3可調節溶液的pH,使得Fe3+和部分Cu2+被除去,當兩種沉淀共存且溶液的pH=8時,c(Cu2+)/ c( Fe3+)=________________ 。
(4)“除銅”反應的離子方程式為________。
(5)若“沉淀”過程中采用Na2C2O4代替(NH4)2C2O4生產草酸鋅晶體,應該在攪拌下,將Na2C2O4溶液緩慢加入ZnCl2溶液中,如果順序顛倒,會產生的不良后果是__________。
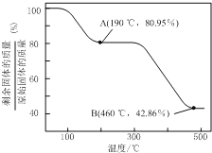
(6)將草酸鋅晶體加熱分解可得到一種納米材料。加熱過程中固體殘留率(剩余固體的質量/原始固體的質量×100%)隨溫度的變化如圖所示,則A、B點固體的化學式分別為____、___________。
【答案】適當提高鹽酸濃度 適當提高反應溫度、適當加快攪拌速率、適當延長酸浸時間(填2條即可) 減小 8.5×1012 ZnS+Cu2+![]() CuS+Zn2+ 產生Zn (OH)2雜質 ZnC2O4 ZnO
CuS+Zn2+ 產生Zn (OH)2雜質 ZnC2O4 ZnO
【解析】
用含主要成分為ZnO,還含有少量Fe2O3,CuO,SiO2和MnO的原料制備草酸鋅晶體,所以制備過程中應當想辦法除去Fe,Cu,Si,Mn等雜質元素;第一步對原料進行酸浸操作,除SiO2不溶于鹽酸外,其余的組分都溶解成相應的金屬陽離子,這一步就將SiO2雜質去除了;接著,向酸浸后的濾液中加入過氧化氫,進行除錳操作,原料中的Mn為+2價,除錳操作獲得的是+4價的錳,所以這一步驟中,Mn被氧化;接著,除鐵步驟利用ZnO調節溶液pH值,將Fe3+除去;除銅步驟,加入的是ZnS,生成CuS,這一步涉及沉淀的轉化反應;最后向溶液中加入草酸銨最終獲得草酸鋅產品。
(1)為了提高浸出率,可以想辦法提高酸浸時的反應速率,或者延長酸浸時間;因此可以提高酸濃度,或者提高溫度,或者充分攪拌等;
(2)除錳步驟中,過氧化氫與溶液中的Mn2+發生氧化還原反應,離子方程式為:![]() ;由于生成了H+,所以溶液的pH減小;
;由于生成了H+,所以溶液的pH減小;
(3)Fe(OH)3和Cu(OH)2兩種沉淀共存時,有:![]() 以及
以及![]() 成立;所以:
成立;所以: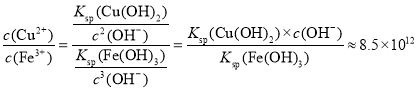 ;
;
(4)除銅時加入的是ZnS,生成的是CuS,發生的反應離子方程式為:![]() ;
;
(5)由于草酸鈉的堿性相比于草酸銨更強,所以若將ZnCl2溶液直接加入草酸鈉溶液中,可能會生成Zn(OH)2雜質;
(6)假設加熱的草酸鋅晶體的初始質量為189g,即1mol;那么根據圖像可知,A點時,固體質量剩余約為153g,失去的質量恰好是草酸鋅晶體中結晶水的質量,所以A點固體的化學式為ZnC2O4;B點時,固體剩余質量約為81g,B點后質量幾乎不再變化,根據質量守恒關系,B點的固體中除65g鋅元素,剩余的即為16gO元素,所以B點固體的化學式為ZnO。


 能力評價系列答案
能力評價系列答案 唐印文化課時測評系列答案
唐印文化課時測評系列答案科目:高中化學 來源: 題型:
【題目】碳酸鎂晶須是一種新型的吸波隱形材料中的增強材料。
(1)合成該物質的步驟如下:
步驟1:配制0.5mol·L-1 MgSO4溶液和0.5mol·L-1 NH4HCO3溶液。
步驟2:用量筒量取500mL NH4HCO3溶液于1000mL三頸燒瓶中,開啟攪拌器。溫度控制在50℃。
步驟3:將250mL MgSO4溶液逐滴加入NH4HCO3溶液中,1min內滴加完后,用氨水調節溶液pH到9.5。
步驟4:放置1h后,過濾,洗滌。
步驟5:在40℃的真空干燥箱中干燥10h,得碳酸鎂晶須產品(MgCO3·nH2O n=1~5)。
①步驟2控制溫度在50℃,較好的加熱方法是_________。
②步驟3生成MgCO3·nH2O沉淀的化學方程式為__________。
③步驟4檢驗沉淀是否洗滌干凈的方法是__________。
(2)測定生成的MgCO3·nH2O中的n值。
稱量1.000碳酸鎂晶須,放入如圖所示的廣口瓶中加入適量水,并滴入稀硫酸與晶須反應,生成的CO2被NaOH溶液吸收,在室溫下反應4~5h,反應后期將溫度升到30℃,最后將燒杯中的溶液用已知濃度的鹽酸滴定,測得CO2的總量;重復上述操作2次。
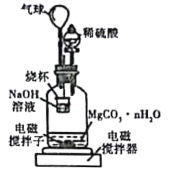
①圖中氣球的作用是_________。
②上述反應后期要升溫到30℃,主要目的是______。
③測得每7.8000g碳酸鎂晶須產生標準狀況下CO2為1.12L,則n值為_______。
(3)碳酸鎂晶須可由菱鎂礦獲得,為測定某菱鎂礦(主要成分是碳酸鎂,含少量碳酸亞鐵、二氧化硅)中鐵的含量,在實驗室分別稱取12.5g菱鎂礦樣品溶于過量的稀硫酸并完全轉移到錐形瓶中,加入指示劑,用0.010mol/L H2O2溶液進行滴定。平行測定四組。消耗H2O2溶液的體積數據如表所示。
實驗編號 | 1 | 2 | 3 | 4 |
消耗H2O2溶液體積/mL | 15.00 | 15.02 | 15.62 | 14.98 |
①H2O2溶液應裝在_________(填“酸式”或“堿式”)滴定管中。
②根據表中數據,可計算出菱鎂礦中鐵元素的質量分數為_________ %(保留小數點后兩位)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C、D、E代表前四周期原子序數依次增大的五種元素。A、D同主族且有兩種常見化合物DA2和DA3;工業上電解熔融C2A3制取單質C;B、E除最外層均只有2個電子外,其余各層全充滿,E位于元素周期表的ds區。回答下列問題:
(1)B、C中第一電離能較大的是________,基態D原子價電子的軌道表達式為________________。
(2)DA2分子的VSEPR模型是____________。
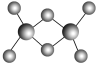
(3)實驗測得C與氯元素形成的化合物的實際組成為C2Cl6,其球棍模型如圖所示。已知C2Cl6在加熱時易升華,與過量的NaOH溶液反應可生成Na[C(OH)4]。
①C2Cl6屬于________(填晶體類型)晶體,其中C原子的雜化軌道類型為________雜化。
②[C(OH)4]-中存在的化學鍵有____________________________________________。
(4)單質A有兩種同素異形體,其中沸點高的是__________ (填分子式),原因是______________________________________________________________
(5)D與E所形成化合物晶體的晶胞如圖所示 。
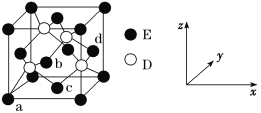
①在該晶胞中,E的配位數為________。
②原子坐標參數可表示晶胞內部各原子的相對位置。如圖晶胞中,原子坐標參數a為(0,0,0);b為(1/2,0,1/2);c為(1/2,1/2,0)。則d的坐標參數為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫時,用0.0200mol/L稀鹽酸滴定20.00mL0.0200mol/LNaY溶液,溶液中水的電離程度隨所加稀鹽酸的體積變化如圖所示(忽略滴定過程中溶液的體積變化或密度變化),則下列有關說法正確的是()
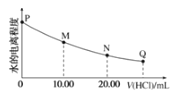
已知:K(HY)=5.0×10-11
A.M點溶液的pH>7
B.M點,c(Na+)=c(HY)+c(Y-)+c(Cl-)
C.可選取酚酞作為滴定指示劑
D.圖中Q點水的電離程度最小,Kw<10-14
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種合成囧烷(E)的路線如下:
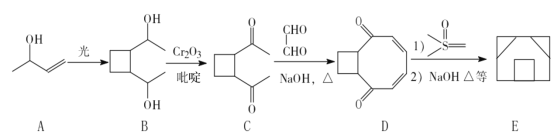
⑴ A中所含官能團的名稱是_______________;E的分子式為_________。
⑵ A→B、B→C的反應類型分別是___________、___________。
⑶ 在一定條件下,B與足量乙酸可發生酯化反應,其化學方程式為______________。
⑷ F是一種芳香族化合物,能同時滿足下列條件的F的同分異構體有_____種。
① 1個F分子比1個C分子少兩個氫原子
② 苯環上有3個取代基
③ 1molF能與2molNaOH反應
寫出其中核磁共振氫譜圖有5組峰,且面積比為3∶2∶2∶2∶1的一種物質的結構簡式:__________。
⑸ 1,2-環己二醇( 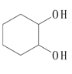 )是一種重要的有機合成原料,請參照題中的合成路線,以
)是一種重要的有機合成原料,請參照題中的合成路線,以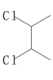 和
和![]() 為主要原料,設計合成1,2-環己二醇的合成路線。______________
為主要原料,設計合成1,2-環己二醇的合成路線。______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某配位化合物為深藍色晶體,由原子序數由小到大的A,B,C,D,E五種元素組成,其原子個數比為14∶4∶5∶1∶1。其中C,D同主族且原子序數D為C的2倍,E元素的外圍電子排布式為(n-1)dn+6ns1,試回答下列問題:
(1)元素B,C,D的第一電離能由大到小排列順序為________(用元素符號表示)。
(2)D元素基態原子的最外層電子排布圖為________。
(3)該配位化合物的化學式為________,配體的中心原子的雜化方式為________。
(4)C元素可與A元素形成兩種常見的化合物,其原子個數比分別為1∶1和1∶2,兩種化合物可以任意比互溶,解釋其主要原因為_______________。
(5)A元素與B元素可形成分子式為B2A2的某化合物,該化合物的分子具有平面結構,則其結構式為________,分子中含有________個σ鍵,________個π鍵。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列由實驗操作得到的實驗現象或結論不正確的是
實驗操作 | 實驗現象或結論 | |
A | 向某溶液中加入稀硫酸,生成淡黃色沉淀和有刺激性氣味的氣體 | 該溶液中一定含有S2O32- |
B | 向3ml KI溶液中滴加幾滴溴水,振蕩,再滴加1mL淀粉溶液,溶液顯藍色 | 氧化性:Br2>I2 |
C | 相同條件下,測定等濃度的Na2CO3溶液和Na2SO4溶液的pH,前者呈堿性,后者呈中性 | 非金屬性:S>C |
D | 將鎂條點燃后迅速伸入集滿CO2的集氣瓶 | 集氣瓶中產生濃煙并有黑色顆粒產生 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是( )
A.常溫下,1.0L pH=13的Ba(OH)2溶液中含有的OH-數目為0.1NA
B.2.0g D216O和H218O混合物中含有的中子數目為0.9NA
C.標準狀況下,22.4L HF中含有NA個HF分子
D.用惰性電極電解CuSO4溶液,若需加入98g Cu(OH)2才能使電解質溶液復原,則電解過程中轉移電子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由丙烯經下列反應制得F、G兩種高分子化合物,它們都是常用的塑料。
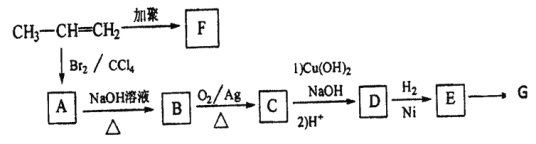
(1)F的結構簡式為________。
(2)在一定條件下,兩分子E能脫去兩分子形成一種六元環狀化合物,該化合物的結構簡式為_______。
(3)①B→C 化學方程式為______。
②C與含有NaOH的Cu(OH)2懸濁液反應的化學方程式為______。
③E→G化學方程式為______。
(4)手性分子X為E的一種同分異構體,lmolX與足量金屬鈉反應產生lmol氫氣,lmolX與足量銀氨溶液反應能生成2molAg,則X的結構簡式為_______。
(5)用G代替F制成一次性塑料餐盒的優點是_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com