
| A. | 鈉和水反應 | B. | 過氧化鈉和水反應 | ||
| C. | 氧化鈉和水反應 | D. | 二氧化碳和水 |
分析 有元素化合價變化的反應為氧化還原反應,水中H、O元素的化合價都沒有變化時水既不做氧化劑又不做還原劑,以此來解答.
解答 解:A.2Na+2H2O═2NaOH+H2↑中,Na元素的化合價升高,水中H元素的化合價降低,屬于氧化還原反應,水作氧化劑,故A錯誤;
B.2Na2O2+2H2O═4NaOH+O2↑中,Na2O2中O元素的化合價既升高又降低,屬于氧化還原反應,水中H、O元素的化合價都沒有變化時水既不做氧化劑又不做還原劑,故B正確;
C.氧化鈉與水的反應為:Na2O+H2O═2NaOH,該反應中沒有化合價變化,不屬于氧化還原反應,故C錯誤;
D.CO2與H2O反應生成H2CO3,該反應中沒有元素的化合價變化,則不屬于氧化還原反應,故D錯誤;
故選B.
點評 本題考查氧化還原反應,為高頻考點,把握反應中元素的化合價變化及氧化還原反應基本概念為解答的關鍵,側重氧化劑、還原劑判斷的考查,題目難度不大.


 同步練習強化拓展系列答案
同步練習強化拓展系列答案科目:高中化學 來源: 題型:選擇題
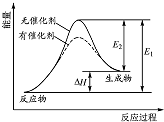
| A. | 該反應的反應物總能量高于生成物總能量 | |
| B. | 使用催化劑可以增大該反應的反應熱 | |
| C. | 該化學反應的反應熱為E1,且反應放熱 | |
| D. | 化學反應在物質變化的同時,必然伴隨能量變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用10 mL 量筒量取 7.50 mL 稀鹽酸 | |
| B. | 用托盤天平稱取 25.20 g NaCl晶體 | |
| C. | 用廣范 pH試紙測得某堿溶液的pH為12.7 | |
| D. | 用25 mL 堿式滴定管量取14.80 mL NaOH 溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4g氫氧化鈉溶于水,電離出的離子總數為2NA | |
| B. | 35.5g氯氣中所含的原子數為2NA | |
| C. | 0.1mol鈉變成鈉離子時,失去的電子數目0.1NA | |
| D. | 實驗室制氯氣,得到2.24L(標準狀況下)氯氣時電子轉移數0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
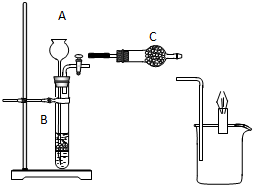 如圖所示裝置中,已知B中隔板上放的是石灰石,若當打開活塞時,燒杯中的蠟燭燃燒得更旺,請回答:
如圖所示裝置中,已知B中隔板上放的是石灰石,若當打開活塞時,燒杯中的蠟燭燃燒得更旺,請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素 | A | B | C | D |
| 相關的原子結構與性質 | 元素符號為At,與稀有氣體元素相鄰,但半徑比I大 | 其在周期表的周期數和族序數比K的均大1 | 元素符號為Tl,名稱是鉈,原子核外有六個電子層,與Al同主族 | 可形成雙原子分子,分子內有叁鍵 |
| A. | 元素A的單質可能是一種有色的固體物質,其氫化物HAt易溶于水,很穩定 | |
| B. | 常溫下B的單質能與冷水發生劇烈反應,其硫酸鹽可能易溶于水 | |
| C. | 鉈氧化物化學式為Tl2O3,是離子化合物,Tl2O3和Tl(OH)3均是兩性的物質 | |
| D. | 元素D的一些氧化物在大氣中會產生光化學煙霧,還會破壞臭氧層 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 海水蒸發制海鹽的過程中只發生了物理變化 | |
| B. | 加入明礬,使海水的鹽分沉淀并淡化 | |
| C. | 海水淡化的方法主要有蒸餾法、離子交換法和電滲析法等 | |
| D. | 大海中含有鉀、溴、碘等元素,需經過氧化還原反應才可得到鉀、溴、碘的單質 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com