
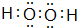 ,其所含化學鍵為(選代碼)bc.
,其所含化學鍵為(選代碼)bc.分析 A、B、C、D是四種短周期元素,它們的原子序數依次增大,A元素的原子只有一個電子層,A與C同主族,則A為H元素;B與D同主族,分別處于二、三周期,二者質子數之和至少為11,兩元素的原子核中質子數之和是A、C兩元素原子核中質子數之和的二倍,C不可能為Li,可推知C為Na;則B、D質子數之和為(1+11)×2=24,令B的質子數為x、則D的質子數為x+8,則x+x+8=22,解得x=8,則B為O元素、D為S元素,符合四種元素的單質常溫常壓下有兩種氣體、兩種固體,據此解答.
解答 解:A、B、C、D是四種短周期元素,它們的原子序數依次增大,A元素的原子只有一個電子層,A與C同主族,則A為H元素;B與D同主族,分別處于二、三周期,二者質子數之和至少為11,兩元素的原子核中質子數之和是A、C兩元素原子核中質子數之和的二倍,C不可能為Li,可推知C為Na;則B、D質子數之和為(1+11)×2=24,令B的質子數為x、則D的質子數為x+8,則x+x+8=22,解得x=8,則B為O元素、D為S元素,符合四種元素的單質常溫常壓下有兩種氣體、兩種固體.
(1)D為S元素,處于周期表中第三周期ⅥA族,由H、O兩種元素可形成E、F兩種化合物,其中一種化合物分解生成另一種化合物,應是H2O2分解生成H2O與O2,該反應方程式為:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,H2O2的電子式是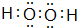 ,分子中H原子與O原子之間形成極性鍵,氧原子之間形成非極性鍵,
,分子中H原子與O原子之間形成極性鍵,氧原子之間形成非極性鍵,
故答案為:第三周期ⅥA族;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;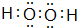 ;bc;
;bc;
(2)①兩元素組成的化合物中S元素為正價,說明O元素對鍵合電子吸引更強,O元素非金屬性強,故①正確;
②單質的熔沸點屬于物理性質,不能比較金屬性強弱,故②錯誤;
③氣態氫化物穩定,中心元素的非金屬性越強,故③正確,
故答案為:①③;
(3)由H、O、S三種元素中的兩種可分別形成甲、乙兩種粒子,它們均為負一價雙原子核的陰離子,且甲含有18個電子,乙含有10個電子,則甲為HS-、乙為OH-,則甲與乙反應的離子方程式為:HS-+OH-=S2-+H2O,
故答案為:HS-+OH-=S2-+H2O;
(4)氫氧化鈉與稀硫酸反應生成硫酸鈉與水,已知此反應生成1molH2O時放出的熱量為57.3kJ,則該反應熱化學方程式為:2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.6kJ/mol,
故答案為:2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l)△H=-114.6kJ/mol;
(5)用氫氣、氧氣制成電池,電池中裝有KOH濃溶液,用多孔的金屬惰性電極浸入KOH溶液,在M極通入氫氣的單質,N極通入氧氣的單質,氫氣發生氧化反應,則M極是該電池的負極;N極發生還原反應,氧氣獲得電子,堿性條件下生成氫氧根,電極反應式為:O2+2H2O+4e-=4OH-,
故答案為:負;O2+2H2O+4e-=4OH-.
點評 本題考查結構性質位置關系應用,涉及電子式、非金屬性強弱比較、熱化學方程式、原電池等,推斷元素是解題關鍵,A為主族元素且有一個電子層為推斷突破口,注意金屬性、非金屬性強弱比較實驗事實,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 在托盤天平兩托盤上各放一片相同的紙,然后將NaOH放在紙片上進行稱量 | |
| B. | 配制溶液時,若加水超過容量瓶刻度,應用膠頭滴管將多余溶液吸出 | |
| C. | 用蒸餾水洗滌燒杯、玻璃棒2-3次,洗滌液也移入容量瓶中 | |
| D. | 定容時俯視容量瓶的刻度線,會造成所配溶液物質的量濃度偏低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
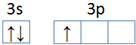 ,第一電離能:鎂大于(填“大于”或“小于”)鋁.
,第一電離能:鎂大于(填“大于”或“小于”)鋁.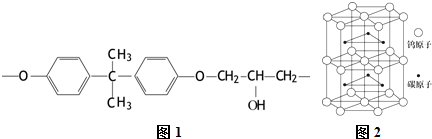
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L的NO2和CO2混合氣體中含有的氧原子數為4NA | |
| B. | 密閉容器中,46gNO2和N2O4的混合氣體所含分子個數為NA | |
| C. | 常溫常壓下,22.4L的液態水含有2.24×10-8NA個OH- | |
| D. | 高溫下,16.8 g Fe與足量水蒸氣完全反應失去0.8NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑C>A>B>D | B. | 價電子數D>C>A>B | ||
| C. | 離子半徑C3+>D->B+>A2+ | D. | 單質的還原性A>B>C>D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
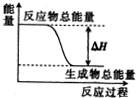
| A. | 灼熱的碳與二氧化碳反應 | |
| B. | 碳酸鈣的分解 | |
| C. | Ba(OH)2•8H2O晶體和NH4Cl晶體混合 | |
| D. | 葡萄糖在人體中轉化成二氧化碳和水 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
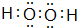 ,其所含化學鍵為(選代碼)bc.
,其所含化學鍵為(選代碼)bc.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃時,pH=13的Ba(OH)2溶液中含有的OH-數目為0.1NA | |
| B. | 粗銅精煉時,當陽極質量減少6.4 g時,電路中轉移的電子數一定不是0.2NA | |
| C. | 含0.2 mol H2SO4的濃硫酸與足量銅反應,生成SO2的分子數為0.1NA | |
| D. | 200 mL 0.5 mol•L-1 Na2CO3溶液中,由于CO32-水解,所以陰離子的數目小于0.1NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com