
| A. | 常溫常壓下,1.7gH2O2中含有的電子數為0.9nA | |
| B. | 1L1 mol.L-1CuCl2溶液含有2nA個Cl- | |
| C. | 1 mol Na 與足量 O2反應,生成Na2O和Na2O2的混合物,鈉失去2nA個電子 | |
| D. | 標準狀況下,2.24L戊烷所含分子數為0.1nA |
分析 A、求出雙氧水的物質的量,然后根據雙氧水中含18個電子來分析;
B、求出氯化銅的物質的量,然后根據1mol氯化銅中含2mol氯離子來分析;
C、根據鈉反應后變為+1價來分析;
D、標況下戊烷為液態.
解答 解:A、1.7g雙氧水的物質的量為0.05mol,而雙氧水中含18個電子,故0.05mol雙氧水中含0.9nA個電子,故A正確;
B、溶液中氯化銅的物質的量n=CV=1mol/L×1L=1mol,而1mol氯化銅中含2mol氯離子,故含2nA個,故B正確;
C、由于鈉反應后變為+1價,故1mol鈉失去nA個電子,故C錯誤;
D、標況下戊烷為液態,故不能根據氣體摩爾體積來計算其物質的量,故D錯誤.
故選AB.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 同一元素不可能既表現金屬性,又表現非金屬性 | |
| B. | 第三周期主族元素的最高正化合價等于它所處的主族序數 | |
| C. | 短周期元素原子形成簡單離子后,最外層電子都達到8電子穩定結構 | |
| D. | 同一主族的元素的原子,最外層電子數相同,化學性質完全相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
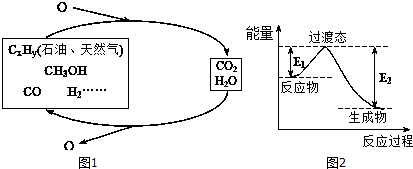
| C-H | C-O | C=O | H-H | H-O |
| 413.4 | 351 | 745 | 436 | 462.8 |
| 實驗 | 溫度/℃ | 起始量 | 達到平衡 | |||
| CO/mol | H2O/mol | H2/mol | CO轉化率 | 所需時間/min | ||
| 1 | 650 | 4 | 2 | 1.6 | 6 | |
| 2 | 900 | 2 | 1 | 1/3 | 3 | |
| 3 | 900 | a | b | c | t | |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石英溶于燒堿溶液:SiO2+2OH-═SiO32-+H2O | |
| B. | 氫氧化鈉溶液中通入少量的二氧化硫:SO2+OH-═HSO3- | |
| C. | 碳酸氫鈣溶液中加入足量氫氧化鈉溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 溴化亞鐵溶液中通入少量氯氣:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 工業上金屬Mg、Cu都是用熱還原法制得的 | |
| B. | 合金的性質與其成分金屬的性質不完全相同 | |
| C. | 金屬冶煉的本質是金屬陽離子得到電子變成金屬原子 | |
| D. | 越活潑的金屬越難冶煉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol Fe與足量H2O(g)反應,轉移的電子數為2NA | |
| B. | 10mL pH=6的純水中含OH-數目為10-10 NA | |
| C. | 1mol羥基中含有的電子數目為9 NA | |
| D. | 100 mL 1 mol/L 的Na2CO3溶液中含有CO32-的數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2摩爾水的摩爾質量和1摩爾水的摩爾質量 | |
| B. | 1mol/L氯化鈣溶液中n(Cl-)和2mol/L氯化鉀溶液中n(Cl-) | |
| C. | 20%NaOH溶液中NaOH的物質的量濃度和10%NaOH溶液中NaOH的物質的量濃度 | |
| D. | 64克二氧化硫中氧原子數和標準狀況下22.4升一氧化碳中氧原子數 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com