
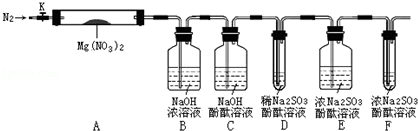
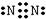 ,步驟Ⅱ中,通入一段時間N2的目的是避免對分解產物O2的檢驗產生干擾.
,步驟Ⅱ中,通入一段時間N2的目的是避免對分解產物O2的檢驗產生干擾.分析 ①根據氧化還原反應中化合價有升高,一定也要降低角度進行判斷;
②氮氣分子中含有氮氮三鍵,最外層滿足8電子穩定結構;各裝置中都有氧氣,避免空氣中氧氣干擾實驗;
③根據二氧化氮為紅棕色氣體分析;
④二氧化氮影響氧氣的檢驗,所以檢驗氧氣前先必須證明二氧化氮已經除盡;
⑤若C中紅色溶液中有氣泡冒出,D中溶液褪色,則證明產物中有氧氣;分別寫出亞硫酸鈉水解、亞硫酸鈉被氧氣氧化的方程式;
⑥根據質量守恒進行判斷;
⑦根據以上分析可知,硝酸鎂分解生成氧化鎂、二氧化氮和氧氣,據此寫出反應的方程式;
⑧空氣中有氧氣,能夠將亞硫酸鈉氧化成硫酸鈉導致溶液質量增加.
解答 解:①Mg(NO3)2受熱分解生成的氮化物中,N元素的化合價降低,則一定有化合價升高的元素,根據硝酸鎂的組成可知,只能為-2價的氧元素失去電子生成氧氣,
故答案為:N元素化合價降低,則一定存在化合價升高的元素,只能為氧元素失去電子生成O2;
②氮氣分子中含有氮氮三鍵,氮原子最外層達到8電子穩定結構,其電子式為: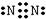 ;
;
步驟Ⅱ中,通入一段時間N2,目的是用氮氣排出裝置中空氣避免對產物氧氣檢驗的干擾,
故答案為: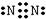 ;避免對分解產物O2的檢驗產生干擾;
;避免對分解產物O2的檢驗產生干擾;
③步驟Ⅲ中,裝置A內若出現了紅棕色氣體,則該紅棕色氣體為NO2,
故答案為:NO2;
④裝置D用于檢驗氧氣,而二氧化氮能夠氧化亞硫酸鈉,影響了氧氣的測定,所以必須用裝置C驗證NO2是否被吸收干凈,防止NO2干擾后續對O2的檢驗,
故答案為:驗證NO2是否被吸收干凈,防止NO2干擾后續對O2的檢驗;
⑤若裝置C中紅色溶液中有氣泡冒出,且試管D中亞硫酸鈉的酚酞溶液褪色,則證明反應產物中有氧氣,涉及的反應有:亞硫酸鈉水解溶液呈堿性,所以滴有酚酞的溶液顯示紅色:Na2SO3+H2O?NaHSO3+NaOH、亞硫酸鈉被氧化生成硫酸鈉:2Na2SO3+O2=2Na2SO4,導致溶液褪色,
故答案為:C中紅色溶液中有氣泡冒出,D中溶液褪色;Na2SO3+H2O?NaHSO3+NaOH、2Na2SO3+O2=2Na2SO4;
⑥稱取3.7gMg(NO3)2固體,反應后剩余1g固體,B中增重2.3g為二氧化氮質量,D、E增重的為氧氣,質量為0.4g,總質量恰好為3.7g,說明反應產物中不會有氮氣生成,
故答案為:Mg(NO3)2的質量與剩余固體、NO2、O2的質量之和相等,已符合質量守恒定律;
⑦取少量剩余固體于試管中,加入適量水,未出現明顯現象,說明反應產物中沒有氮化鎂和亞硝酸鎂,只能為氧化鎂,結合其它分析可知,硝酸鎂分解生成氧化鎂、二氧化氮氣體和氧氣,反應方程式為:2Mg(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+4NO2↑+O2↑,
故答案為:2Mg(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2MgO+4NO2↑+O2↑;
⑧裝置F的作用是吸收空氣中氧氣,避免干擾實驗測定,由于亞硫酸鈉與空氣中氧氣反應生成硫酸鈉,導致試管F中溶液質量增加,
故答案為:吸收空氣進入的O2所致.
點評 本題考查了性質實驗方案的設計,題目難度中等,明確實驗原理及化學實驗基本操作方法為解答關鍵,注意掌握物質的性質及檢驗方法,試題側重考查學生的分析、理解能力及化學實驗能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 合成氨工業中,移走NH3可增大正反應速率,提高原料轉化率 | |
| B. | 酸堿中和滴定時,錐形瓶需用待測液潤洗2~3次,再加入待測液 | |
| C. | 將NO2、N2O4混合氣體的體積壓縮為原來的一半,則氣體顏色加深 | |
| D. | 電解精煉銅過程中,陽極質量的減少與陰極質量的增加一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 7:8 | C. | 8:7 | D. | 5:4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 裝置 | 現象 | 結論及解釋 |
 | ①A試管中黑色沉淀逐漸溶解 ②A試管上方出現紅棕色氣體 ③B試管中出現白色沉淀 | a.現象②說明褐色沉淀具有 還原性. b.試管B中產生白色沉淀的總反應的離子方程式為 NO2+SO2+Ba2++H2O═BaSO4↓+NO↑+2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com