


 口算能手系列答案
口算能手系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
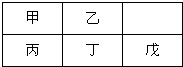 短周期金屬元素甲-戊在元素周期表中的相對位置如圖,下列判斷正確的是( )
短周期金屬元素甲-戊在元素周期表中的相對位置如圖,下列判斷正確的是( )| A、原子半徑:丙<丁<戊 |
| B、戊只與強堿反應 |
| C、最高價氧化物對應水化物堿性:乙>丁>戊 |
| D、金屬性:丙>甲 |
查看答案和解析>>
科目:高中化學 來源: 題型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、滴加石蕊顯紅色的溶液中:Na+、Fe2+、Cl-、NO3- | ||
B、
| ||
| C、c(H+)=10-12 mol?L-1的溶液:K+、Ba2+、Cl-、Br- | ||
| D、由水電離的c(H+)=1.0×10-13 mol?L-1的溶液中:K+、NH4+、AlO2-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:
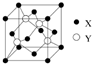 元素X位于第四周期,其基態原子的內層軌道全部排滿電子,且最外層電子數為1.元素Y基態原子的3p軌道上有5個電子.元素Z的原子最外層電子數是其內層的3倍.元素W基態原子的核外電子共有16種運動狀態.
元素X位于第四周期,其基態原子的內層軌道全部排滿電子,且最外層電子數為1.元素Y基態原子的3p軌道上有5個電子.元素Z的原子最外層電子數是其內層的3倍.元素W基態原子的核外電子共有16種運動狀態.查看答案和解析>>
科目:高中化學 來源: 題型:
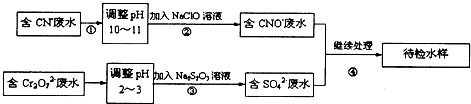
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com